2 квітня, 2025
Особливості ліпідознижувальної терапії у пацієнтів високого та дуже високого кардіоваскулярного ризику
Серцево-судинні захворювання (ССЗ) є незмінним лідером серед причин смертності в усьому світі та в Україні зокрема. Так, у 2021 році смертність через ССЗ, включаючи ішемічну хворобу серця (ІХС), становила 418 випадків на 100 тис. населення. Пацієнти з гострим коронарним синдромом (ГКС) на тлі ІХС потребують особливої уваги, оскільки вони є одним із головних факторів у структурі загальної та серцево-судинної смертності, випадків госпіталізації, економічного навантаження на країну. З огляду на це заходи вторинної профілактики щодо виникнення повторних епізодів ГКС, зокрема корекція ліпідного профілю, є наріжним каменем у веденні такої категорії хворих.
ГКС – сукупність клінічних симптомів, які проявляються гострою ішемією міокарда при порушенні його кровопостачання внаслідок зменшення кровотоку в коронарних артеріях. ГКС зазвичай зумовлюється руйнуванням (розривом або ерозією) нестабільної атеросклеротичної бляшки коронарної артерії з асоційованим частковим чи повним тромбозом коронарної артерії та/або мікроемболією, що спричиняє зниження кровотоку й подальшу ішемію міокарда (Libby, 2013; Falk et al., 2013). ГКС включає 3 пов’язані клінічні стани, що існують уздовж континууму тяжкості: нестабільну стенокардію, інфаркт міокарда (ІМ) без підйому сегмента ST (NSTEMI) та ІМ із підйомом сегмента ST і наявністю чи відсутністю зубця Q (STEMI).
В пацієнтів із нещодавнім ГКС частота подій, пов’язаних з атеросклеротичними ССЗ (АССЗ), є значно вищою, ніж у хворих із хронічними кардіоваскулярними захворюваннями, причому частота серцево-судинної смерті, ІМ, ішемічного інсульту становить від 10 до 15% упродовж року після ГКС (Ulvenstam et al., 2023; Steen et al., 2022). Вищий ризик серед пацієнтів із ГКС потребує жорсткішої тактики в досягненні цільових показників холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) у пацієнтів із нещодавнім ГКС порівняно із хворими з ІХС (Virani et al., 2023; Ulvenstam et al., 2023; Steen et al., 2022). Результати рандомізованих клінічних досліджень (РКД) продемонстрували зменшення атеросклеротичних серцево-судинних подій за допомогою різних фармакологічних підходів до зниження рівня ХС ЛПНЩ, при цьому величина користі напряму залежала від ступеня зниження рівня ХС ЛПНЩ (Baigent et al., 2010).
Групи ризику та цілі лікування
У настановах із лікування дисліпідемій Європейського товариства кардіологів (ESC) та Європейського товариства з атеросклерозу (EAS) 2019 р. наголошено на необхідності подальшого зменшення ХС ЛПНЩ у хворих груп високого і дуже високого ризику на основі отриманих висновків про те, що нижчі рівні ХС ЛПНЩ є кращими за вищі й не спричиняють жодних небажаних ефектів (Mach et al., 2020).
До групи високого серцево-судинного ризику належать:
- виражені окремі фактори ризику: загальний холестерин >8 ммоль/л, ХС ЛПНЩ >4,9 ммоль/л або артеріальний тиск >180/110 мм рт. ст.;
- пацієнти із сімейною гіперхолестеринемією без інших основних ризиків;
- хворі на цукровий діабет без ураження органів-мішеней або з додатковими факторами ризику;
- хронічна хвороба нирок з помірним порушенням функції (швидкість клубочкової фільтрації (ШКФ) 30-59 мл/хв/1,73 м²);
- показник за шкалою SCORE (Systematic COronary Risk Evaluation) від 5 до 10% для 10-річного ризику летального ССЗ.
Група дуже високого серцево-судинного ризику характеризується:
- наявністю задокументованих АССЗ (наприклад, ІМ, інсульт, стабільна стенокардія);
- виявленням значних атеросклеротичних змін при візуалізації (наприклад, бляшки на коронарній ангіографії або УЗД сонних артерій);
- хронічною хворобою нирок із тяжким порушенням функції (ШКФ <30 мл/хв/1,73 м²);
- показником SCORE >10% для 10-річного ризику фатальних ССЗ;
- генетично зумовленою гіперхолестеринемією з іншими значними факторами ризику.
До пацієнтів екстремального ризику належать:
- хворі з повторними серцево-судинними подіями протягом 2 років, незважаючи на оптимальну терапію;
- особи із множинними факторами ризику, як-от тяжка гіперхолестеринемія, неконтрольована артеріальна гіпертензія та цукровий діабет;
- пацієнти після ГКС з анамнезом інших васкулярних подій / хвороби периферійних артерій / поліваскулярного ураження / багатосудинного ураження коронарних артерій / сімейної гіперхолестеринемії.
Цільові рівні ХС ЛПНЩ для осіб із високим ризиком становлять <1,8 ммоль/л (<70 мг/дл), для дуже високого ризику – зниження ХС ЛПНЩ не менше ніж на 50% початкового, цільовий рівень – <1,4 ммоль/л (<55 мг/дл). Водночас для пацієнтів із ССЗ, які переживають повторний судинний напад протягом 2 років (не обов’язково того самого типу, що і перший) на тлі приймання статинів у максимально переносимій дозі, рекомендовано знизити рівень ХС ЛПНЩ <1,0 ммоль/л (<40 мг/дл) (ESC/EAS, 2019).
Високоінтенсивна статинотерапія
Статини – добре відомі препарати першої лінії для зменшення вмісту ХС ЛПНЩ. У сучасних клінічних настановах, у рекомендаціях ESC (2019) зазначено, що першим кроком лікування дисліпідемії має бути титрування дози статину до максимальної або максимально переносимої. Другим кроком передбачено додавання комбінованої терапії з різним класом показань залежно від клінічної ситуації у разі недосягнення цільового рівня ХС ЛПНЩ на тлі приймання статинів високої інтенсивності.
У пацієнтів із ГКС РКД продемонстрували додаткові переваги терапії статинами високої інтенсивності порівняно з помірною інтенсивністю щодо зниження серйозних серцево-судинних подій (MACE) (Schwartz et al., 2001; de Lemos et al., 2004; Cannon et al., 2004; Baigent et al., 2010). Варто зазначити, що разом із ліпідознижувальною дією застосування статинів забезпечує антиагрегантний і протизапальний ефекти, а також поліпшення функції ендотелію (Xie et al., 2024), що особливо важливо в пацієнтів із ГКС.
Високоінтенсивне лікування статинами знижує концентрацію ХС ЛПНЩ на ≥50%. Метааналіз 5 РКД показав, що зниження концентрації ХС ЛПНЩ за участю статинів високої інтенсивності порівняно зі статинами помірної інтенсивності зменшує основні судинні події на ≈15% у пацієнтів з ІХС (Baigent et al., 2010). Метааналіз окремих учасників досліджень The A to Z та PROVE IT-TIMI 22, обидва з яких проводилися в пацієнтів, стан яких стабілізувався на ранніх стадіях після ГКС, продемонстрував значне зниження серцево-судинної та смертності від усіх причин за інтенсивніших режимів статинів порівняно з менш інтенсивними (Murphy et al., 2007). Користь високоінтенсивного режиму статинів проявляється досить рано після ГКС і зберігається протягом тривалого часу та не залежить від базової концентрації ХС ЛПНЩ, тому корекція ліпідного профілю є особливо важливою на ранніх етапах госпіталізації пацієнтів із ГКС (Cannon et al., 2004).
Ознак будь-яких занепокоєнь щодо безпеки від досягнення дуже низьких концентрацій ХС ЛПНЩ при застосуванні статинів або інших гіполіпідемічних методів лікування не спостерігалося; отже, високоінтенсивну терапію статинами не слід зменшувати під час подальшого спостереження в хворих, які добре переносять лікування (Wiviott et al., 2005).
Алгоритм терапії у пацієнтів із високим ризиком
Монотерапія статинами, навіть високоінтенсивними, в більшості пацієнтів не дозволяє досягти цільових рівнів ХС ЛПНЩ, рекомендованих у настановах. Оскільки кардіопротекторний ефект зниження ХС ЛПНЩ не залежить від конкретного механізму дії препарату, це відкриває можливість усунути розрив між рекомендаціями та реальними досягнутими показниками в клінічній практиці. Однак для цього необхідні суттєві зміни в підходах до лікування та більш прагматичне мислення. Тому пропонується змінити парадигму терапії для пацієнтів із дуже високим кардіоваскулярним ризиком, переходячи від підходу «спочатку інтенсивна терапія статинами» до концепції інтенсивної ліпідознижувальної терапії. Це означає, що в таких пацієнтів зниження ХС ЛПНЩ має відбуватися максимально ефективно, без зволікань і з використанням усіх доступних можливостей.
За останнє десятиліття клінічні дослідження ліпідознижувальної терапії дозволили точно оцінити середнє зниження рівня ХС ЛПНЩ для кожного типу лікування. Це дало змогу розробити спрощений алгоритм терапії для пацієнтів із дуже високим ризиком, що дозволяє ефективно контролювати рівень ХС ЛПНЩ (рис. 1).
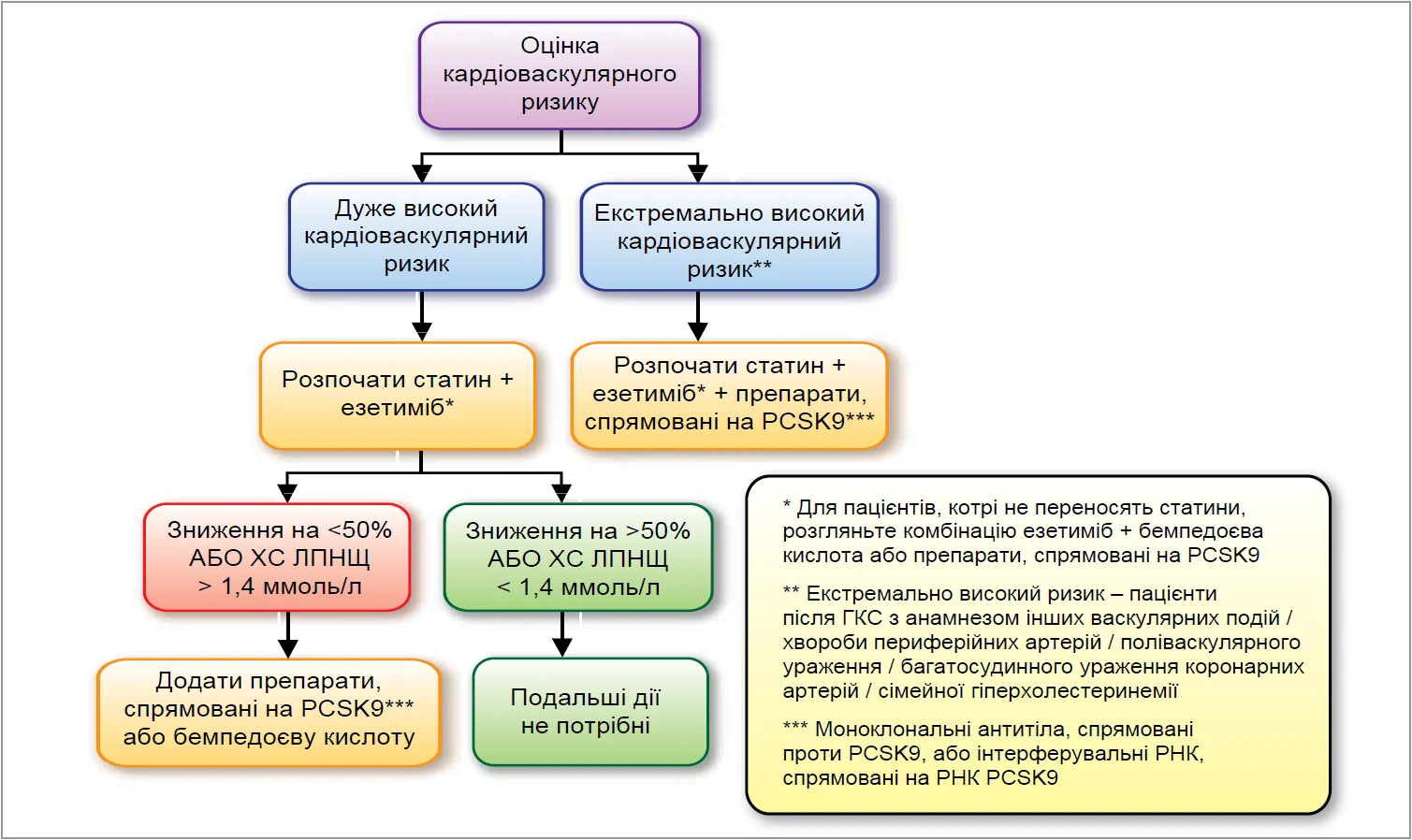 Рис. 1. Комбінована ЛЗТ як стратегія першої лінії для пацієнтів високого та дуже високого ризику (адаптовано за Ray K.K. et al., 2021)
Рис. 1. Комбінована ЛЗТ як стратегія першої лінії для пацієнтів високого та дуже високого ризику (адаптовано за Ray K.K. et al., 2021)
Примітка: PCSK9 – інгібітори пропротеїнової конвертази субтилізин-кексинового типу.
Перший крок у такому підході полягає в стартовій комбінації статину та езетимібу, що забезпечує раннє значне зниження рівня ХС ЛПНЩ на понад 50% і має стати стандартом клінічної практики. Якщо цільових рівнів ЛПНЩ, рекомендованих у настановах 2019 року (зниження >50% і концентрація <1,4 ммоль/л), не досягнуто, слід додати третій ліпідознижувальний препарат, такий як бемпедоєва кислота або інгібітори PCSK9 (моноклональні антитіла проти PCSK9 або PCSK9 siRNA).
Для пацієнтів із непереносимістю статинів також рекомендується комбінована терапія на першому етапі, наприклад поєднання езетимібу з бемпедоєвою кислотою або з інгібіторами PCSK9. Такий підхід дозволяє забезпечити ефективне індивідуалізоване зниження ЛПНЩ відповідно до сучасних рекомендацій.
Комбінована терапія
Нерідко виникають ситуації, коли застосування високодозової статинотерапії недостатньо для досягнення цільових рівнів ХС ЛПНЩ або пацієнти погано переносять статини. В таких випадках необхідно розглянути комбіновану ліпідознижувальну терапію.
Непереносимість статинів часто зустрічається в клінічній практиці; найпоширенішим проявом є м’язові симптоми, пов’язані зі статинотерапією (Bytyci et al., 2022). Для встановлення факту непереносимості статинів необхідно підтвердження виникнення зазначених симптомів на тлі приймання щонайменше двох статинів, включно зі щонайменше одним у найнижчій затвердженій добовій дозі (Cheeley et al., 2022). Наразі для пацієнтів із повною або частковою непереносимістю статинів доступні варіанти включають езетиміб, моноклональні антитіла до інгібітора PCSK9, інклісиран та бемпедоєву кислоту. Було продемонстровано, що езетиміб і PCSK9 є безпечними та добре переносяться, а також покращують ліпідні параметри в пацієнтів із непереносимістю статинів (Moriarty et al., 2015; Nissen et al., 2016).
Згідно з останніми рекомендаціями AHA/ACC/ACCP/ASPC/NLA/PCNA (2023), для пацієнтів, які не досягли цільового рівня ХС ЛПНЩ при максимально переносимій терапії статинами, а також для хворих, котрі не переносять статинів, доцільно застосовувати нестатинові препарати, як-от езетиміб, оскільки вони можуть знизити як рівні ХС ЛПНЩ, так і ризик MACE (Cannon et al., 2015; Schwartz et al., 2018; Sabatine et al., 2017; Moriarty et al., 2015; Nissen et al., 2016, 2023).
Нині доступні численні терапевтичні варіанти, які можна додати до максимально переносимої терапії статинами для досягнення бажаних цілей ХС ЛПНЩ у пацієнтів із ГКС. Езетиміб знижує рівень ХС ЛПНЩ на 15-25%, блокуючи його всмоктування зі шлунково-кишкового тракту за допомогою білка Niemann-Pick C 1-Like 1 (NPC 1L1), додатково знижуючи рівень ХС ЛПНЩ на 23-24% при застосуванні разом зі статинами (Cannon et al., 2015). Під час проведення дослідження IMPROVE IT вивчали комбінацію симвастатину (40 мг) й езетимібу (10 мг) (симвастатин/езетиміб) порівняно із симвастатином (40 мг) і плацебо (монотерапія симвастатином) у пацієнтів, госпіталізованих із ГКС протягом останніх 10 днів. Середній час від ГКС до рандомізації становив 5 днів, при цьому 34% пацієнтів уже приймали статини на момент події ГКС. Додавання езетимібу знизило відносний ризик MACE на 6,4% протягом 6 років спостереження. Езетиміб добре переносився (Cannon et al., 2015).
Клінічні дослідження інгібіторів PCSK9 продемонстрували 15% зниження відносного ризику MACE в середньому від 2 до 3 років, включаючи пацієнтів >1 міс після ГКС (Schwartz et al., 2018; Sabatine et al., 2017; Gencer et al., 2020). Еволокумаб ефективно знижує рівень ХС ЛПНЩ на ранній стадії після ГКС; він продемонстрував сприятливі зміни компонентів бляшок, визначені за допомогою внутрішньокоронарної візуалізації у пацієнтів із NSTEMI (Koskinas et al., 2019; Leucker et al., 2020; Nicholls et al., 2022).
Інклісиран – це невелика інтерферувальна РНК, спрямована на пригнічення синтезу білка PCSK9, яку вводять із 6-місячними інтервалами після початкової 3-місячної дози. Інклісиран знижує рівень ХС ЛПНЩ на ≈50% і добре переноситься (Ray et al., 2020), але результати досліджень щодо клінічних ефектів наразі недоступні. Бемпедоєва кислота зумовлює ≈20% зниження рівня ХС ЛПНЩ; знижує MACE на 13% у пацієнтів із непереносимістю статинів, якщо її застосування розпочинати >90 днів після ГКС (Nissen et al., 2023).
Серед зазначених можливих комбінацій найдослідженішою, найбезпечнішою та економічно доступною є комбінація езетимібу і статинів. Метою рандомізованого обсерваційного дослідження RACING було порівняння ефективності та безпеки високоінтенсивної монотерапії розувастатином та комбінованої терапії (розувастатин/езетиміб) для пацієнтів з атеросклеротичними ССЗ, яким був імплантований стент із медикаметозним покриттям (n=72 050). Зокрема, 10 794 пацієнти отримували комбіновану терапію (розувастатин 10 мг плюс езетиміб 10 мг), 61 256 пацієнтів – монотерапію розувастатином (20 мг). Первинною кінцевою точкою була комбінована частота серцево-судинної смерті, ІМ, реваскуляризації коронарної артерії, госпіталізації для лікування серцевої недостатності та нефатального інсульту впродовж 3-річного періоду спостереження. Дослідження показало, що комбінована гіполіпідемічна терапія була пов’язана з меншою частотою первинної кінцевої точки (11,6 проти 15,2% для групи монотерапії; відношення ризиків (ВР) 0,75; 95% ДІ 0,70-0,79; p<0,001) (рис. 2).
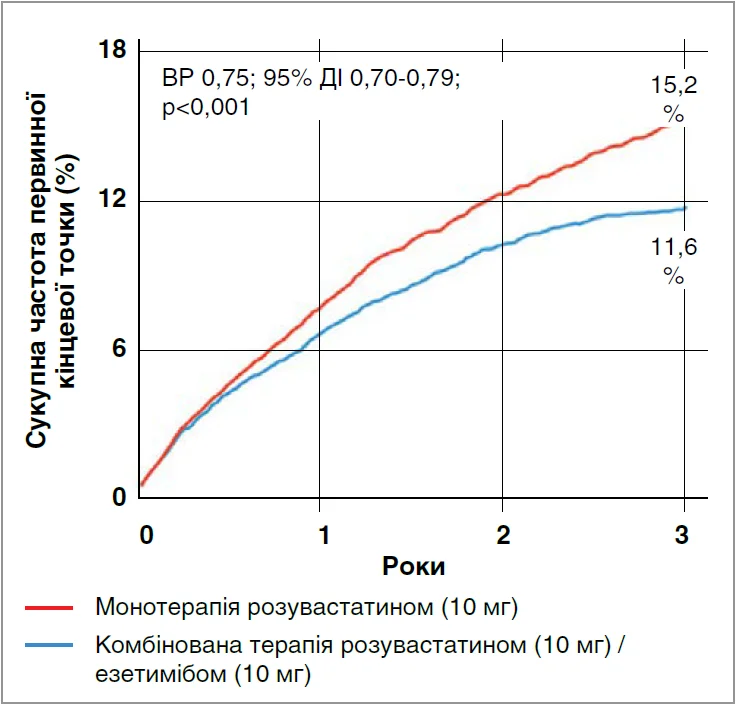 Рис. 2. Сукупна частота первинної кінцевої точки (серцево-судинна смерть, ІМ, реваскуляризації коронарної артерії, серцева недостатність або нефатальний інсульт) протягом 3-річного періоду спостереження в межах дослідження RACING (адаптовано за Lee S.-J. et al., 2023)
Рис. 2. Сукупна частота первинної кінцевої точки (серцево-судинна смерть, ІМ, реваскуляризації коронарної артерії, серцева недостатність або нефатальний інсульт) протягом 3-річного періоду спостереження в межах дослідження RACING (адаптовано за Lee S.-J. et al., 2023)
Порівняно з монотерапією статинами високої інтенсивності комбінована гіполіпідемічна терапія характеризувалася меншою кількістю припинень лікування (6,5 проти 7,6%; ВР 0,85; 95% ДІ 0,78-0,94; p<0,001) і меншою частотою нових випадків цукрового діабету (7,7 проти 9,6%; ВР 0,80; 95% ДІ 0,72-0,88; p<0,001). Комбінована ліпідознижувальна терапія розувастатином та езетимібом асоціювалася зі сприятливими клінічними результатами та дотриманням режиму лікування пацієнтів з імплантованим стентом із медикаментозним покриттям (Lee et al., 2023).
Застосування комбінованої терапії з фіксованою дозою за допомогою твердих капсул
Нині у фармації широко застосовують технології, які дають змогу створювати удосконалені форми лікарських препаратів. Такою є технологія «дуопіл»: поєднання двох окремих таблеток, кожна з яких створена за своєю технологією, в одній капсулі. У тверді капсули можна вміщувати порошки, гранули, міні-/мікротаблетки або менші капсули – у більшу. Ці комбінації можуть містити кілька активних фармацевтичних інгредієнтів (АФІ), щоб уникнути проблем несумісності, пов’язаних із певними препаратами. Меншу капсулу можна інкапсулювати в більшу, що дасть можливість ефективно розділити дві речовини та зберегти їх синергетичний ефект. У такий спосіб вдається вирішити не тільки питання несумісності, але й утворення домішок через взаємодію АФІ, оскільки між препаратами немає контакту. Залежно від вимог до рецептури, дві або більше активні речовини можна комбінувати у формі пелет, мікротаблеток або порошків. Ця комбінація надає пацієнтам можливість приймати препарат раз на добу, що сприяє поліпшенню прихильності до лікування. Ще одна перевага полягає в тому, що можна досягти комбінації різних параметрів профілю вивільнення (один препарат може бути у формі з негайним вивільненням, а інший – із модифікованим або кожен у складі комбінації може бути розроблений для вивільнення в різних ділянках шлунково-кишкового тракту). Це може бути досягнуто завдяки використанню декількох таблеток із різними покриттями для забезпечення кількох профілів вивільнення препарату.
З огляду на нижчі цільові показники ХС ЛПНЩ у пацієнтів дуже високого та екстремального серцево-судинного ризику ліпідознижувальну терапію для цієї категорії осіб доцільно розпочинати із комбінації статину й езетимібу. Так, згідно з рекомендаціями ESC та EAS, комбінована терапія, яка включає статини й езетиміб, є ефективнішою за монотерапію для досягнення цільових рівнів ХС ЛПНЩ. Комбінована терапія із застосуванням статину та езетимібу також забезпечує швидше досягнення цільових показників, що є критично важливим для пацієнтів з екстремальним ризиком (клас рекомендації І, рівень доказів В).
Загалом застосування комбінації ліпідознижувальних препаратів із фіксованою дозою в 1 таблетці сприяє ефективнішому зниженню рівня ХС ЛПНЩ порівняно з монотерапією, а також покращує прихильність до лікування (Katzmann et al., 2020). Поєднання статину та езетимібу в 1 таблетці підвищує прихильність до ліпідознижувальної терапії у пацієнтів різних вікових груп та з різними рівнями серцево-судинного ризику (Rea et al., 2021).
Отже, лікування пацієнтів із дуже високим та екстремальним серцево-судинним ризиком необхідно розпочинати із застосування комбінованої ліпідознижувальної терапії, що забезпечує ефективне й швидке досягнення цільових рівнів ХС ЛПНЩ і профілактує MACE. Комбінована терапія статином та езетимібом рекомендована пацієнтам із високим і дуже високим та екстремальним ризиком як основний стандарт лікування для досягнення більш раннього зниження >50% ХС ЛПНЩ. На відміну від високоінтенсивної статинотерапії, застосування фіксованих комбінацій статину й езетимібу асоційовано із кращою прихильністю та меншою частотою відмови від лікування.
На ринку України комбінація розувастатину й езетимібу представлена препаратом Розуліп® Плюс у дозуванні (розувастатин/езетиміб) 10/10 та 20/10 мг.
Підготувала Людмила Суржко
Медична газета «Здоров’я України 21 сторіччя» № 5 (591), 2025 р



