24 серпня, 2024
Новітні результати досліджень застосування цефоперазону/сульбактаму у пацієнтів ВІТ
Негоспітальна пневмонія (НП), і зокрема тяжка НП (ТНП), є значною причиною захворюваності та смерті. Незважаючи на розвиток і вдосконалення лікування (Leoni D. et al., 2017), рівень летальності серед пацієнтів із НП залишається високим і коливається від 17% до понад 50% (Phua J. et al., 2016). Одним із важливих аспектів у лікуванні таких пацієнтів є емпіричне призначення оптимальної антибіотикотерапїі з урахуванням можливої етіології НП. Ще однією проблемою, з якою стикаються лікарі відділень інтенсивної терапії (ВІТ), є зростання частоти внутрішньолікарняних інфекцій, спричинених Klebsiella pneumoniae, що продукує b-лактамази розширеного спектра дії. Нещодавно були опублікувані результати багатоцентрових клінічних досліджень, одне з яких порівнювало результати лікування цефоперазоном/сульбактамом та піперациліном/тазобактамом у хворих із ТНП, а інше – оцінювало ефективність і безпеку цефоперазону/сульбактаму у пацієнтів із бактеріємією, спричиненою K. pneumoniae.
Ключові слова: негоспітальна пневмонія, цефоперазон/сульбактам, піперацилін/тазобактам, бактеріємія, Klebsiella pneumoniae, мінімальна інгібуюча концентрація.
Клінічна ефективність цефоперазону/сульбактаму порівняно з піперациліном/тазобактамом у лікуванні тяжкої негоспітальної пневмонії
Згідно з рекомендаціями Американського торакального товариства (ATS)/Американського товариства з інфекційних хвороб (IDSA), ТНП визначається за наступними клінічними ознаками:
- наявність ≥1 з основних критеріїв, включаючи інвазивну механічну вентиляцію й/або септичний шок;
- наявність ≥3 із другорядних критеріїв, у тому числі:
- частота дихання ≥30 вдихів/хв;
- парціальний тиск кисню (PaO2)/частка вдихуваного кисню (FiO2) ≤250 мм рт. ст.;
- множинні лобарні інфільтрати;
- сплутаність свідомості;
- концентрація азоту в сечовині крові ≥20 мг/дл;
- кількість лейкоцитів <4000 клітин/мм3;
- кількість тромбоцитів <10 000 клітин/мм3;
- температура тіла <36 °C і/або гіпотензія.
Streptococcus pneumoniae залишається найпоширенішим збудником НП, а також частою причиною ТНП, що зазвичай призводить до госпіталізації у ВІТ [7, 8]. Haemophilus influenza, Legionella pneumonia та Influenza pneumonia є збудниками, які також спричиняють ТНП у ВІТ [9, 10]. Проте близько 6% мікроорганізмів, які не належать до основних збудників НП (умовно називаються PES – Pseudomonas aeruginosa, Enterobacteriaceae, що продукують β-лактамази розширеного спектра [БЛРС], і метицилін-резистентний Staphylococcus aureus), також можуть спричиняти тяжкі захворювання [11], а частота неадекватного застосування емпіричних антибіотиків є дуже високою.
Важливо визначити фактори ризику інфікування PES, щоб вибрати відповідне антибіотикотерапевтичне лікування. Основними компонентами оцінки вірогідності PES є: вік >65 років, чоловіча стать, попереднє застосування антибіотиків, наявність хронічних респіраторних захворювань, хронічної патології нирок, порушення свідомості та лихоманка [12]. T. Maruyama et al. (2019) запропонували стратегію антибіотикотерапії пневмонії, яка базується не на локалізації інфекції, а на факторах ризику збудників PES [13]. Використання емпіричних антибіотиків широкого спектра дії, які охоплюють збудників PES, слід розглядати для покращення результатів лікування, особливо в пацієнтів з показником PES ≥5 [14].
Цефоперазон/сульбактам є антибактеріальним засобом широкого спектра, що активний проти найпоширеніших респіраторних патогенів і мультирезистентних організмів, включаючи представників родини Enterobacteriaceae, P. aeruginosa, інші не ферментуючі глюкозу грамнегативні палички та анаероби [15]. Доказові дані свідчать, що цефоперазон/сульбактам не поступається цефепіму та піперациліну/тазобактаму за ефективністю лікування внутрішньолікарняної пневмонії та пневмонії, пов’язаної з наданням медичної допомоги [16, 17], проте дослідження щодо клінічної ефективності цефоперазону/сульбактаму в лікуванні ТНП відсутні.
Матеріали та методи
Це дослідження є багатоцентровим ретроспективним аналізом клінічної ефективності та безпечності цефоперазону/сульбактаму в лікуванні пацієнтів, які страждають на ТНП. Дослідження проводилося з березня 2018 року по травень 2019 року у восьми медичних центрах та одній регіональній клініці Тайваню. Пацієнти, включені в дослідження, отримували цефоперазон/сульбактам або піперацилін/тазобактам для лікування ТНП, внутрішньолікарняної та вентилятор-асоційованої пневмонії. Дані були зібрані ретроспективно з електронних медичних карт.
Для цілей дослідження пневмонія визначалась як наявність ≥2 респіраторних симптомів і ознак (включаючи кашель, лихоманку, гіпотермію, гнійне мокротиння або виділення з дихальних шляхів) та характерні зміни на рентгенограмі органів грудної клітки за інтерпретацією лікаря [18]. Діагноз ТНП ґрунтувався на рекомендаціях ATS/IDSA [4]. Виділення з дихальних шляхів і посіви крові відбиралися перед призначенням антибіотиків.
Первинною кінцевою точкою ефективності була клінічна частота виліковування атипової пневмонії у відповідь на призначення антибіотиків. Таким чином, частота одужання визначалася як частка пацієнтів, у яких клінічні симптоми чи ознаки зникли або покращилися через 7 днів після закінчення антибіотикотерапії без додаткового лікування.
На противагу цьому клінічна невдача була визначена наступним чином: клінічні симптоми або ознаки погіршилися або зберігалися після 3-5 днів антибіотикотерапії й вимагали додаткового призначення антибіотиків для лікування; смерть від пневмонії після 3-5 днів антибіотикотерапії; або прогресування пневмонії та розвиток емпієми чи абсцесу легені.
Невизначені результати включали переведення до інших медичних закладів, відмову від подальшого лікування, смерть від пневмонії після менш ніж 2 днів антибіотикотерапії, незавершене лікування через алергію, серйозні побічні ефекти або інші причини.
Вторинні результати включали клінічну ефективність, ризик побічних ефектів та госпітальну смерть.
Клінічну ефективність визначали як покращення клінічних симптомів й ознак, рентгенографічної картини та вираженості запалення, включаючи рівні лейкоцитів, прокальцитоніну, С-реактивного білка. На противагу цьому клінічна неефективність визначалася у разі недосягнення жодного із трьох вищезазначених критеріїв. Невизначена ефективність визначалася як така, що не може бути оцінена за трьома вищезазначеними критеріями.
Результати
Демографічні дані
Загалом було залучено 815 пацієнтів із НП, які отримували антибіотики. Учасники були розподілені у дві групи лікування: перша група отримувала цефоперазон/сульбактам (n=343), а друга група – піперацилін-тазобактам (n=472). Середній вік пацієнтів у групі цефоперазону/сульбактаму становив 74,78±15,00 року, і більшість (70,6%) із них були чоловіками. Середня тривалість лікування цефоперазоном/сульбактамом становила 9,08±3,53 дня. Подібні вихідні дані були й у групі піперациліну/тазобактаму, включаючи відомості щодо віку, статі та тривалості антибіотикотерапії. Однак індекс коморбідності Чарлсона був значно вищим у групі цефоперазону/сульбактаму порівняно з групою піперациліну/тазобактаму (6,20±2,77 проти 5,72±2,61 відповідно; р=0,009). На противагу цьому не було достовірних відмінностей між двома групами за показниками індексу тяжкості пневмонії або за шкалою CURB‑65 (шкала тяжкості НП).
Крім того, різниця в частоті ідентифікації мікроорганізмів між двома групами не була статистично значущою (49,7% проти 49,6% відповідно; р=0,981). У групі цефоперазону/сульбактаму найчастіше виявляли K. pneumoniae (11,1%) та P. aeruginosa (6,4%). Подібні результати спостерігалися і в групі піперациліну/тазобактаму. Двома найпоширенішими збудниками були P. aeruginosa (8,6%) та K. pneumonia (8,2%).
pneumoniae не був найпоширенішим збудником у пацієнтів із ТНП у цьому дослідженні (4,8%). Щодо небажаних явищ, пов’язаних із лікуванням, то 21 пацієнту, які отримували цефоперазон/сульбактам, було проведено визначення міжнародного нормалізованого відношення (МНВ) до або через 1 тиждень після терапії. У цих пацієнтів не було виявлено достовірної різниці між показниками МНВ до та після лікування (1,14 проти 1,13; р=0,597).
У 8,7% (71/815) пацієнтів із ТНП були виявлені збудники PES. Багато вихідних характеристик в обох групах були подібними, включаючи вік, стать та основні супутні захворювання; однак поширеність хронічних захворювань легень була вищою серед пацієнтів із PES (36,6% проти 25,8%; р=0,049). Не було достовірних відмінностей за індексом коморбідності Чарлсона, балами за шкалою APACHE II (фізіологічна оцінка гострих і хронічних захворювань), показниками шкали SOFA (оцінка органної недостатності) та qSOFA (швидка оцінка SOFA) при порівнянні хворих із PES і без PES. Незважаючи на ці обставини показник клінічного одужання пацієнтів у підгрупі PES був значно нижчим, ніж в інших хворих (73,2% проти 82,9%; р=0,021). Показник госпітальної смерті серед пацієнтів із PES також був вищим порівняно з іншими хворими (26,8% проти 16,1%; р=0,023).
Ефективність лікування
Первинні результати частоти клінічного одужання та частоти невдач (або невизначений результат) між групами цефоперазону/сульбактаму та піперациліну/тазобактаму становили 84,2% проти 80,3% і 15,7% проти 19,7% відповідно (р=0,367). Що стосується вторинних результатів, то показники клінічної ефективності та неефективності (або невизначений результат) цефоперазону/сульбактаму становили 85,4% і 14,5%, що було зіставно з показниками у групі піперациліну/тазобактаму (83,3% і 16,7%; р=0,258). Крім того, рівень госпітальної летальності був подібним між групами цефоперазону/сульбактаму та піперациліну/тазобактаму (16,0% проти 17,8%; р=0,572).
З іншого боку, відповідно до оцінки вихідного стану хворих за шкалою Чарлсона, тяжкість захворювання відрізнялася між двома групами. Для коригування впливу цього фактора на кінцевий результат був застосований метод оцінки схильності. Частота клінічного одужання при призначенні цефоперазону/сульбактаму була вищою, ніж при застосуванні піперациліну/тазобактаму (85,4% проти 79,3%; р=0,041) (скориговане відношення шансів [ВШ] 1,53; 95% довірчий інтервал [ДІ] 1,02-2,31). Не було виявлено достовірної різниці між двома групами щодо вторинних результатів або госпітальної смерті (рисунок).
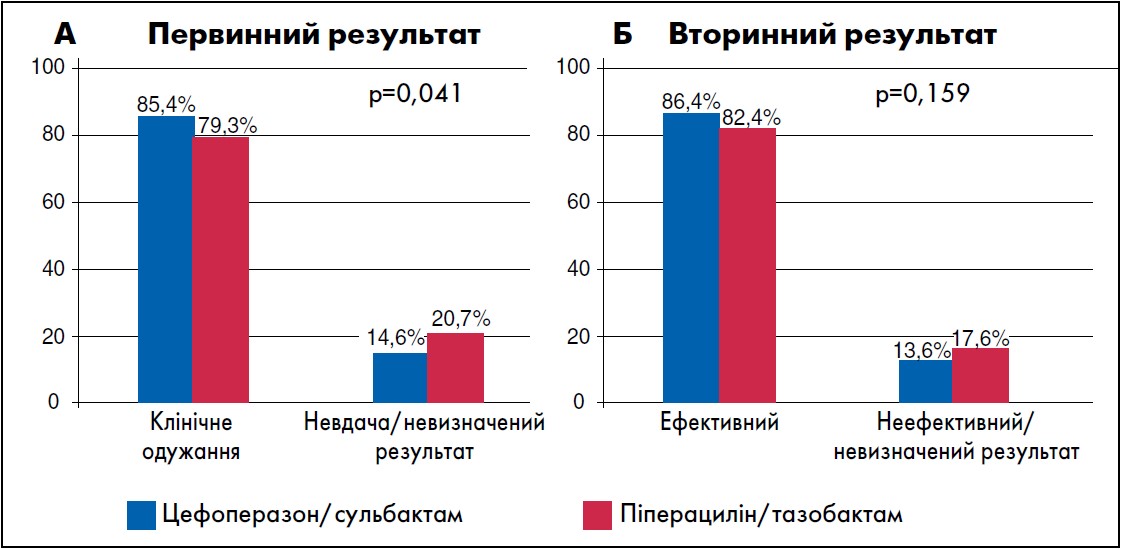
Рис. Первинний (А) і вторинний (Б) результати пацієнтів, які отримували цефоперазон/сульбактам та піперацилін/тазобактам для терапії ТНП після коригування показника схильності до лікування
Обговорення
Початково при лікуванні ТНП клінічні показники одужання та ефективності цефоперазону/сульбактаму були зіставними з показниками піперациліну/тазобактаму. Однак цефоперазон/сульбактам продемонстрував кращі клінічні первинні результати після коригування за шкалою Чарлсона. Внутрішньолікарняна смерть була порівнянною у пацієнтів, які отримували будь-який із цих двох антибіотиків. Збудники PES частіше виявлялися у пацієнтів із хронічними захворюваннями легень, і ці пацієнти, як правило, мали несприятливі результати.
У даному дослідженні P. aeruginosa (7,7%) і K. pneumoniae (9,3%) були найпоширенішими збудниками, що призводили до ТНП. За ними йшли E. coli (6,3%), Acinetobacter spp. (5,0%) та S. pneumoniae (4,7%). Показники госпітальної летальності у пацієнтів із НП, які отримували цефоперазон/сульбактам та піперацилін/тазобактам, становили 16,0% і 17,8% відповідно; однак госпітальна летальність у пацієнтів із ТНП, викликаною PES-збудниками, була вищою, ніж у пацієнтів без PES-збудників (26,8% проти 16,1%; р=0,023). У досліджуваній когорті рівень летальності був нижчим у пацієнтів із ТНП порівняно з попередніми дослідженнями, що свідчить про те, що антибіотики широкого спектра дії можуть бути ефективнішими в лікуванні хворих на ТНП.
Цефоперазон ефективний не тільки проти грампозитивних аеробів, а й проти широкого спектра грамнегативних аеробів, включаючи представників родини Enterobacteriaceae, P. aeruginosa та інших грамнегативних паличок, що не ферментують глюкозу, in vitro [21]. Однак на його мінімальну інгібуючу концентрацію (МІК) впливає висока концентрація бактерій, що продукують β-лактамазу [21]. У поєднанні із сульбактамом ефект бактеріальної стійкості проти цефоперазону можна подолати [22] і, таким чином, збільшити додаткове покриття анаеробів [23]. Крім того, сульбактам має власну антибактеріальну активність щодо деяких штамів Acinetobacter [24].
У дослідженні S.S. Jean et al. чутливість E. coli, K. pneumoniae, Citrobacter freundii, Serratia marcescens, Proteus mirabilis, P. aeruginosa, Enterobacter cloacae та Acinetobacter spp. до цефоперазону/сульбактаму перевищувала 85% [25]. В іншому дослідженні було встановлено, що чутливість до цефоперазону/сульбактаму стійких до антибіотиків БЛРС E. coli становила 97%, БЛРС K. pneumoniae – 75,8% і карбапенем-резистентної A. baumannii – 68% [22]. Піперацилін/тазобактам був найпоширенішим антибіотиком, який призначали при підозрі на резистентність збудників, але було показано, що він має несприятливі наслідки у пацієнтів із бактеріємією, спричиненою E. coli та K. pneumoniae [26].
Дане дослідження продемонструвало вищий рівень клінічного одужання при застосуванні цефоперазону/сульбактаму порівняно з піперациліном/тазобактамом після коригування за тяжкістю для ТНП. На основі вищезазначених досліджень було доведено, що цефоперазон/сульбактам є ще одним альтернативним антибіотиком, який можна використовувати для боротьби з антибіотикорезистентними бактеріями.
З іншого боку, при призначенні цефоперазону/сульбактаму слід враховувати міркування безпеки: коагулопатія, зумовлена бічним ланцюгом N-метилтіотетразолу, потенційно може спричиняти транзиторну гіпопротромбінемію [27]. Це ускладнення, як правило, є рідкісним і спостерігається лише у пацієнтів, які одночасно отримують антикоагулянти, в осіб із недостатнім харчуванням та в тих, хто переніс геморагічні явища впродовж останніх півроку [28]. У цьому дослідженні у 21 пацієнта, який отримував цефоперазон, не було виявлено суттєвої різниці в показниках МНВ до та після лікування; однак більшість пацієнтів не проходили рутинного обстеження на предмет порушень згортання крові, оскільки в цьому ретроспективному дослідженні у них не спостерігалося значних кровотеч.
Попередні результати дослідження ефективності цефоперазону/сульбактаму у хворих із бактеріємією, спричиненою K. pneumoniae
pneumoniae є поширеним і загрозливим для життя збудником внутрішньолікарняних інфекцій. K. pneumoniae може викликати пневмонію, інфекції сечовивідних шляхів, внутрішньочеревні інфекції, абсцеси печінки, бактеріємію та інші інфекції [1-3]. Смертність пацієнтів із бактеріємією, спричиненою K. pneumoniae, може сягати 20-50%, залежно від інфікованої популяції та тяжкості інфекції [4-6].
Цефоперазон – цефалоспорин 3-го покоління, активний проти грампозитивних коків і грамнегативних бактерій, за винятком штамів, що продукують БЛРС [10-12]. Додавання сульбактаму, сульфону пеніциланової кислоти з активністю проти ферментів класу А за класифікацією Амблера, розширило антимікробний спектр цефоперазону [13, 14].
У минулому поява K. pneumoniae, що продукує БЛРС, спричиняла серйозну клінічну проблему [7-9]. За даними програми антимікробного нагляду SENTRY, поширеність мультирезистентних ентеробактеріальних інфекцій, асоційованих з інфекціями кровотоку, зросла з 6,2 до 15,8% у період із 1997 по 2016 рік [9]. Комбінація цефоперазону/сульбактаму активна проти багатьох мультирезистентних грамнегативних бактерій, включаючи ентеробактерії, що продукують БЛРС, P. aeruginosa і A. baumannii [16, 17]. Вона ефективна у хворих із фебрильною нейтропенією, внутрішньочеревними інфекціями, НП і госпітальною пневмонією, спричиненими мультирезистентними грамнегативними збудниками [12, 18-22]. Однак наразі не встановлені МІК для інтерпретації клінічних порогових значень МІК для комбінації цефоперазону (1,0)/сульбактаму (1,0) відповідно до рекомендацій Інституту клінічних і лабораторних стандартів та Європейського комітету з тестування антимікробної чутливості [23, 24].
Матеріали та методи
Це багатоцентрове дослідження проводилося з липня 2017 по вересень 2022 року у восьми медичних центрах Тайваню. Учасники – пацієнти віком >20 років, які мали мономікробну бактеріємію, спричинену K. pneumoniae. Початково вони отримували антимікробну монотерапію із застосуванням цефоперазону/сульбактаму протягом 24 год від початку бактеріємії, при цьому лікування тривало понад 72 год [25, 27].
Цефоперазон/сульбактам уводили внутрішньовенно кожні 12 год із модифікацією дозування відповідно до рекомендацій виробника, згідно з оцінкою кліренсу креатиніну за рівнянням Кокрофта – Голта [28]. Усі пацієнти, які отримували додаткову антимікробну терапію понад 48 год, були виключені з дослідження, за винятком тих, хто потребував протигрибкової або противірусної терапії чи антибактеріальних препаратів, спрямованих саме проти грампозитивних коків.
Для оцінки супутніх захворювань використовували індекс коморбідності Чарлсона, для оцінки тяжкості захворювання – шкалу APACHE II та шкалу бактеріємії за Піттом. Через 30 днів оцінювали клінічні результати, які поділялися на чотири категорії: одужання, покращення, відсутність ефективності та смерть.
Одужання визначалося як відсутність симптомів і ознак інфекції без потреби в додатковій антибіотикотерапії та негативний результат наступного посіву крові протягом тижня від початку бактеріємії. Покращення означало, що симптоми та ознаки зникли (із лабораторним покращенням або без нього) на основі клінічної оцінки, і пацієнти потребували подальшого лікування антибіотиками. Відсутність ефективності визначалася як клінічне прогресування, летальний кінець або персистуюча бактеріємія наприкінці лікування цефоперазоном/сульбактамом [29]. Щодо кореляції між ефективністю лікування та МІК цефоперазону/сульбактаму, то одужання та покращення були визначені як сприятливі результати. І навпаки, відсутність ефективності та смерть були визначені як несприятливі результати.
Результати
Протягом періоду дослідження було включено 201 пацієнта з бактеріємією, спричиненою K. pneumoniae, відповідно до критеріїв відбору. Середній вік становив 69 років. Більшість пацієнтів були чоловіками (n=124, 61,69%). Найпоширенішими супутніми захворюваннями були цукровий діабет (n=77, 38,31%), порушення функції печінки (n=61, 30,35%) і порушення функції нирок (n=41, 20,40%). Основною причиною бактеріємії була внутрішньочеревна інфекція (n=65, 32,34%), за якою слідували первинна бактеріємія (n=64, 31,84%), інфекції дихальних шляхів (n=33, 16,42%) та сечовивідних шляхів (n=28, 13,93%).
Серед 201 ізоляту 180 (89,55%) були чутливими, 6 (2,99%) – проміжними і 15 (7,46%) – резистентними до цефоперазону/сульбактаму. Ізоляти K. pneumoniae були чутливішими до цефоперазону/сульбактаму, ніж до цефоперазону. В ізолятів, які не були чутливими до цефоперазону, додавання сульбактаму відновило рівень чутливості з 0 до 53,33% і знизило рівень резистентності з 82,22 до 33,33%. Більшість ізолятів K. pneumoniae у цьому дослідженні мали МІК <8 мкг/мл.
Оцінка результатів показала, що 156 (77,61%) пацієнтів мали сприятливі результати (одужання та покращення), а 45 (22,39%) хворих – несприятливі: смерть (n=24, 11,94%) і відсутність ефективності лікування (n=21, 10,45%). Зі збільшенням значення МІК частота сприятливих результатів зменшувалася, а 30-денна летальність зростала.
При багатофакторному аналізі такі показники, як більш високий бал за шкалою APACHE II (відношення шансів [ВШ] 1,14; 95% довірчий інтервал [ДІ] 1,07-1,21; р<0,001), метастатичні пухлини (ВШ 5,76; 95% ДІ 2,31-14,40; р<0,001) та інфекція, зумовлена ізолятами K. pneumoniae, із МІК цефоперазону/сульбактаму >16 мкг/мл (ВШ 4,30; 95% ДІ 1,50-12,27; р=0,006) були незалежно пов’язані з несприятливими наслідками.
Обговорення
Це перше багатоцентрове дослідження, у якому вивчалися ефекти терапії цефоперазоном/сульбактамом у пацієнтів із бактеріємією, спричиненою K. pneumoniae, визначалися клінічні порогові значення та прогностичні фактори щодо результатів. Кореляційний аналіз рівнів МІК цефоперазону/сульбактаму щодо K. pneumoniae з клінічними наслідками показав, що більшість пацієнтів (81,1%) із МІК ≤16 мкг/мл мали сприятливі результати. Значення МІК >16 мкг/ мл незалежно асоціювалися з несприятливими наслідками. Крім того, вищі бали за шкалою APACHE II та наявність метастатичного раку також були негативними прогностичними факторами в пацієнтів із бактеріємією, спричиненою K. pneumoniae.
Основним механізмом, що лежить в основі резистентності K. pneumoniae до цефалоспоринів 3-го покоління, є наявність генів БЛРС [30, 31]. Застосування карбапенемів зросло, що сприяло поширенню карбапенем-резистентної K. pneumoniae [32, 33]. У цьому випадку цефоперазон/сульбактам може забезпечити альтернативну карбапенем-зберігаючу терапію, що є цінним досягненням в антимікробному менеджменті.
Як показало дане дослідження, МІК цефоперазону/сульбактаму >16 мкг/мл була пов’язана з несприятливими наслідками, що вказує на те, що таким пацієнтам із бактеріємією, спричиненою K. pneumoniae, не слід призначати цей антибіотик. На противагу цьому в більшості пацієнтів із МІК ≤16 мкг/мл спостерігалися сприятливі результати (81,1%). Це свідчить про те, що незважаючи на появу резистентності цефоперазон/сульбактам зберігає хорошу антимікробну ефективність.
Це дослідження показало, що оцінка за шкалою APACHE ІІ та наявність метастатичних пухлин були значущими факторами ризику несприятливого результату, що узгоджується з результатами попередніх досліджень бактеріємії, спричиненої K. pneumoniae, у яких повідомлялося про подібний зв’язок [39, 40]. Тому виважене антимікробне лікування є важливим у пацієнтів із такими факторами ризику. Для впевненої оцінки ефективності цефоперазону/сульбактаму в лікуванні бактеріємії, спричиненої K. pneumoniae, слід зосередити увагу на моніторингу ізолятів із МІК ≤16 мкг/мл.
Висновки
На сьогодні не втрачає актуальності проблема вибору емпіричної антибіотикотерапії у пацієнтів ВІТ із діагнозом ТНП. Хоча S. pneumoniae залишається найпоширенішим збудником НП, а також частою причиною ТНП, у пацієнтів ВІТ із ТНП на перший план виходять K. pneumoniae та P. aeruginosa. Поряд із тим важливе значення щодо несприятливого прогнозу у хворих із ТНП має виявлення в них мікроорганізмів групи PES (P. aeruginosa, Enterobacteriaceae, що продукують БЛРС, і метицилін-резистентний S. aureus).
Клінічна ефективність цефоперазону/сульбактаму в лікуванні дорослих пацієнтів із ТНП була зіставною з ефективністю піперациліну/тазобактаму. Водночас, після коригування за ступенем тяжкості захворювання, частота клінічного одужання при призначенні цефоперазону/сульбактаму була вищою, ніж при застосуванні піперациліну/тазобактаму.
pneumoniae, як один із найпоширеніших і життєзагрозливих збудників внутрішньолікарняних інфекцій, є причиною бактеріємії, смертність за якої може сягати від 20 до 50% випадків. Призначення пацієнтам із бактеріємією, зумовленою K. рneumoniae, цефоперазону/сульбактаму мало найбільш сприятливий результат, коли МІК препарату становила ≤16 мкг/мл. Факторами, що погіршували результат лікування, були вищі бали за шкалою APACHE II та наявність метастатичного раку.
Реферативний огляд підготувала Дар’я Чорна
За матеріалами: Lai C.-C., Chen W.-C., Kuo L.-K. et al.
The clinical efficacy of cefoperazone-sulbactam versus
piperacillin-tazobactam in the treatment of severe community-acquired pneumonia. Medicine 2023;102:28(e34284); Chiang T.-T., Chiang M.-H. et al. Multicenter study on clinical outcomes and risk factors in patients with Klebsiella pneumonia bacteremia receiving cefoperazone/sulbactam treatment. https://doi.org/10.21203/rs.3.rs‑3982160/v1.
Тематичний номер «Хірургія. Ортопедія. Травматологія. Інтенсивна терапія» № 3 (60), 2024 р.



