13 вересня, 2024
Залишковий серцево-судинний ризик: роль залишкового холестерину, співвідношення моноцитів/ЛПВЩ та ліпопротеїнів в індивідуальній профілактиці серцево-судинних захворювань
 Серцево-судинні хвороби є основною причиною смертності у світі та мають обмежені методи профілактики, незважаючи на використання ефективних препаратів. Поняття залишкового ризику (ЗР) нерозривно пов’язане з поняттям глобального ризику, в якому воно становить дуже значний відсоток. У сфері серцево-судинного здоров’я термін «ЗР» означає ймовірність виникнення серйозної серцево-судинної події, незважаючи на адекватний контроль чинників ризику, присутніх у конкретного пацієнта.
Серцево-судинні хвороби є основною причиною смертності у світі та мають обмежені методи профілактики, незважаючи на використання ефективних препаратів. Поняття залишкового ризику (ЗР) нерозривно пов’язане з поняттям глобального ризику, в якому воно становить дуже значний відсоток. У сфері серцево-судинного здоров’я термін «ЗР» означає ймовірність виникнення серйозної серцево-судинної події, незважаючи на адекватний контроль чинників ризику, присутніх у конкретного пацієнта.
Залишковий серцево-судинний ризик – це ймовірність розвитку серйозної серцево-судинної події після того, як пацієнт отримує лікування, рекомендоване стандартами медичної допомоги [1]. Цей показник має декілька складових:
- ризик, пов’язаний із відомими та невідомими, але немодифікованими чинниками (вік, стать, етнічна приналежність, генетична схильність);
- ризик, пов’язаний із чинниками, які відомі й піддаються модифікації, але не повністю кореговані (рівень ліпопротеїнів високої щільності (ЛПВЩ) і тригліцеридів (ТГ), абдомінальне ожиріння, артеріальний тиск, інсулінорезистентність, куріння тощо).
Дисліпідемія відповідає приблизно за 55% ризику розвитку інфаркту міокарда. Серцево-судинні хвороби є основною причиною захворюваності та смертності в усьому світі, а дисліпідемія є значним чинником ризику [2]. Основною характеристикою дисліпідемії є підвищення рівня холестерину ліпопротеїнів низької щільності (ЛПНЩ), що тісно пов’язане з підвищеним ризиком серцево-судинних захворювань, зокрема атеросклеротичних [3, 4]. Численні епідеміологічні, клінічні й експериментальні дослідження підкреслили критичну важливість холестерину ЛПНЩ, включаючи його окислену форму, як основного каталізатора розвитку атеросклерозу [5]. Отже, зниження рівня холестерину ЛПНЩ є одним із найпоширеніших підходів у клінічній практиці для лікування та профілактики атеросклеротичних серцево-судинних захворювань [6].
Терапія статинами є наріжним каменем цього лікування й клінічних досліджень, у яких вони використовувалися для первинної та вторинної профілактики. Хоча було підкреслено, що відзначається зниження відносного ризику серцево-судинних подій після лікування, пацієнт залишається вразливими до значного ЗР.
Стійкі порушення ліпідного профілю, незважаючи на лікування статинами, роблять значний внесок у ЗР серцево-судинних захворювань, а отже, підкреслюють клінічну важливість прийняття терапевтичних рішень, які не обмежуються зниженням рівня холестерину ЛПНЩ, але також впливають на рівень холестерину ЛПВЩ і ТГ [7].
Залишковий серцево-судинний ризик: нові дані
Традиційні чинники ризику самі по собі не можуть повністю пояснити високий вплив коронарних подій у ефективно лікованих пацієнтів. Насправді класичні калькулятори для оцінювання серцево-судинного ризику, які враховують лише традиційні чинники ризику, як-от Фрамінгемська шкала, можуть недооцінювати ризик у певній конкретній популяції [8]. Через це потрібно також виокремлювати нові чинники серцево-судинного ризику, що з’являються (рис.).
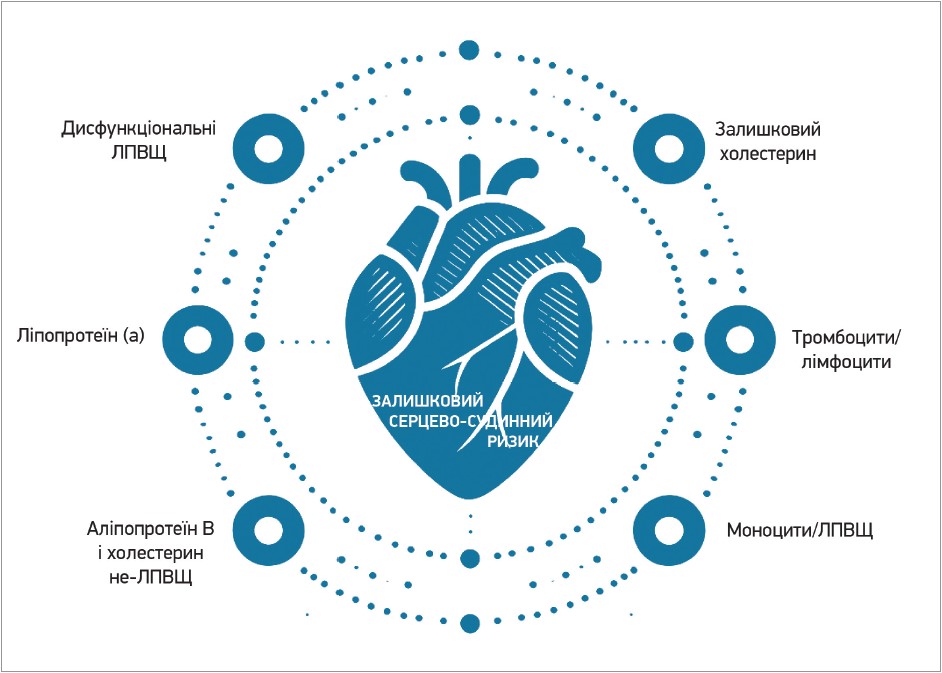
Рис. Залишковий серцево-судинний ризик
Дисфункціональні ЛПВЩ
Дисфункціональні ЛПВЩ – це частинки холестерину ЛПВЩ із високими проатерогенними властивостями, що характеризуються втратою типових антиоксидантних властивостей і стають переносниками окислених ліпідів. У ранніх дослідженнях підкреслювалася важливість розрізнення втрати функції ЛПВЩ і набуття дисфункції. Було відзначено, що ЛПВЩ можуть втрачати протизапальні властивості й навіть розвивати прозапальні характеристики. Однак є випадки, коли здатність ЛПВЩ доставляти ефіри холестерину через рецептор SCARB1 може бути знижена, що вказує лише на часткову втрату функції. Подальші дослідження показали, що ступінь втрати нормальної функції ЛПВЩ і посилення дисфункції може варіювати залежно від різних біологічних активностей. Деякі дослідження вказують на повну втрату функції та посилення дисфункції щодо протизапальної, судинорозширювальної й антиапоптотичної активностей. Утім, коли йдеться про антиоксидантну активність і здатність виведення холестерину, дефіцит, який спостерігається при нормальній функції ЛПВЩ, не доходить до повної дисфункції [9].
Ліпопротеїн (а)
Частинка ліпопротеїну (а) нагадує ЛПНЩ за своїм багатим на холестерин складом і складається з аполіпопротеїну В, ковалентно пов’язаного з аполіпопротеїном (а). Відзначається його значний зв’язок із серцево-судинним ризиком, атеросклерозом та ішемічною хворобою серця (ІХС) [10, 11]. Підвищений рівень ліпопротеїну (а) асоціюється з підвищеним ризиком коронарних і цереброваскулярних подій, хворобами периферичних артерій, серцевою недостатністю та фібриляцією передсердь [12].
Нещодавня класифікація рівнів ліпопротеїну (а) передбачає, що показник <30 мг/дл (<75 нмоль/л) указує на нижчий серцево-судинний ризик, тоді як рівні від 30 до 50 мг/дл (75-125 нмоль/л) становлять сіру зону з погляду ризику [12]. Існують розбіжності щодо впливу статинів на рівень ліпопротеїну (а), причому деякі дослідження свідчать про його підвищення в пацієнтів, які отримують статини, особливо в тих, хто має низький фенотип аполіпопротеїну (а). Проте статини мають вирішальне значення для пацієнтів із підвищеним рівнем ліпопротеїну (а) через їхню ефективність в інтенсивному зниженні ЛПНЩ [12]. Ніацин завдяки різним механізмам знижує рівень частинок, що містять аполіпопротеїн В, тому було запропоновано впливати інгібіторами PCSK9 на рівень ліпопротеїну (а) поряд із терапією ніацином. Клінічні дослідження показали середнє зниження відсотка ліпопротеїну (а) при застосуванні інгібіторів ферменту PCSK9, але це зниження не сприяє зменшенню серцево-судинних подій [14, 15]. Комбінована терапія ніацином і статинами створює підвищений ризик побічних ефектів.
Нові методи лікування, спрямовані на мРНК аполіпопротеїну (а), як-от пелакарсен та олпасиран, демонструють значне зниження рівнів ліпопротеїну (а) без значних проблем із безпекою. Клінічні випробування цих препаратів показують багатонадійні результати в зниженні серцево-судинних подій.
Залишковий холестерин
Кілька клінічних досліджень продемонстрували, що в пацієнтів із дисліпідемією, які отримують гіполіпідемічну терапію, значний залишковий серцево-судинний ризик продовжує зберігатися, незважаючи на досягнення цільових значень холестерину ЛПНЩ. Є припущення, що це пов’язано з наявністю високих рівнів у плазмі крові ліпопротеїнів, багатих на ТГ, і залишкового холестерину (ЗХ).
Концентрація ЛПНЩ тісно пов’язана з показниками тригліцеридемії, а серцево-судинний ризик, пов’язаний із цими ліпопротеїнами, зумовлений тим, що вони гідролізуються до частинок ЗХ. Останні є ліпопротеїнами, багатими на ефіри холестерину, меншими за розміром, ніж ЛПНЩ, і тому вважається, що вони мають атерогенний вплив, подібний до ліпопротеїнів дуже низької щільності (ЛПДНЩ), але насправді концентрація ЗХ у плазмі крові пов’язана із серцево-судинним ризиком незалежно від рівня холестерину ЛПНЩ.
У деяких дослідженнях, проведених за участю понад 90 тис. осіб із загальної популяції Данії протягом 22 років, було виявлено, що прогресивне збільшення значень ЗХ, виміряних у пацієнтів, які не голодують, достовірно корелювало з підвищеним ризиком розвитку ІХС і гострих коронарних подій, а також із загальною смертністю. Крім того, було підкреслено, що особи зі значеннями ЗХ >43 мг/дл мали у 2-3 рази більший ризик ІХС порівняно з особами зі значеннями <15 мг/дл.
A.J. Vallejo-Vaz і співавт. виявили, що показники ЗХ у пацієнтів, які страждають на ІХС, достовірно корелювали з розвитком основних несприятливих серцево-судинних подій (ОНССП) [11]. Однак зниження на 1 стандартне відхилення показників ЗХ після лікування аторвастатином сприяло зменшенню частоти виникнення ОНССП незалежно від зниження рівня холестерину ЛПНЩ [24].
Співвідношення моноцитів/ЛПВЩ
Співвідношення моноцитів до холестерину ЛПВЩ (СМЛ), що розраховується шляхом ділення кількості моноцитів у периферичній крові на рівень холестерину ЛПВЩ, є сучасним показником системного запалення, а також вважається предиктором серцево-судинних подій. Моноцити беруть участь у вивільненні прозапальних і прооксидантних цитокінів у місцях запалення, відіграючи важливу роль у хронічному запаленні та серцево-судинних захворюваннях.
Окрім того, ці запальні клітини є основними клітинами, які інфільтрують артеріальну стінку в початкових стадіях атерогенезу. І навпаки, холестерин ЛПВЩ має протизапальний і антиоксидантний ефекти, які виражаються через пригнічення продукції та мобілізації моноцитів, а також через блокування міграції макрофагів у артеріальній стінці та виведення молекул холестерину з цих клітин.
Зокрема, було визначено, що СМЛ, який дорівнює 12,1, здатний точно прогнозувати наявність гемодинамічно значущих коронарних стенозів [27].
S.K. Açıkgöz і співавт. підкреслили корисність СМЛ як незалежного предиктора госпітальної та довгострокової (протягом 5 років) смертності, а також ОНССП у пацієнтів з інфарктом міокарда з підйомом сегмента ST. Пацієнти були розподілені на три групи з огляду на зростання значень СМЛ, вищий ризик смертності й ОНССП мали пацієнти, які належали до третьої групи (СМЛ – 30,1). Було виявлено, що СМЛ є незалежним предиктором 30-денної смертності в пацієнтів з інсультом (із граничним значенням 17,5, здатним адекватно прогнозувати цю смертність) [30].
Нарешті, значення СМЛ порівнювали між пацієнтами з метаболічним синдромом і здоровими особами. Це співвідношення було значно збільшене в пацієнтів порівняно з групою контролю (13,9 проти 11,1). Було виявлено, що СМЛ є незалежним предиктором наявності метаболічного синдрому й може бути використане як новий індикатор цього клінічного стану [31].
Співвідношення тромбоцитів до лімфоцитів
Тромбоцити дійсно відіграють значну роль у розвитку, дестабілізації та розриві атеросклеротичних бляшок. І навпаки, кількість лімфоцитів слугує індикатором фізіологічного стресу й має зворотний зв’язок із запаленням: зменшення кількості лімфоцитів визначає збільшення серцево-судинного ризику та смертності. Співвідношення тромбоцитів і лімфоцитів (СТЛ), що розраховується шляхом ділення кількості тромбоцитів на кількість лімфоцитів, є новим прогностичним маркером, який об’єднує властивості цих двох параметрів в один. Він надає інформацію про шляхи агрегації тромбоцитів і запалення й може бути кориснішим і надійнішим у прогнозуванні серцево-судинного ризику та коронарного пошкодження, ніж кількість тромбоцитів або лімфоцитів, розглянуті окремо [32].
Ayça та співавт. оцінили прогностичне значення СТЛ у 440 пацієнтів з інфарктом міокарда з підйомом сегмента ST, яким було проведено первинну ангіопластику. Пацієнти були розподілені на дві групи на підставі низьких (<137) і високих значень СТЛ (>137). Пацієнти з високими значеннями СТЛ мали більшу частоту феномену no-reflow і смертності, а також вищі значення за шкалою Syntax (шкала анатомічної оцінки тяжкості уражень коронарних артерій), що свідчить про тяжчий і складніший перебіг коронарної хвороби [33].
Zhou та співавт. вивчали потенційну кореляцію між СТЛ і тяжкістю ІХС, а також клінічними наслідками після черезшкірного коронарного втручання в китайській популяції з діагнозом інфаркту міокарда з підйомом сегмента ST. Результати дослідження показали, що СТЛ демонструє незалежний зв’язок як з тяжкістю ІХС, так і з виникненням довгострокових ОНССП після черезшкірного коронарного втручання [34]. Пацієнти з СТЛ >171 мали вираженіший коронарний стеноз і гірший прогноз, а також вищу частоту виникнення ОНССП протягом 5-річного спостереження. Отже, зрозуміло, наскільки високі значення СТЛ можна вважати предикторами тяжкої та складної коронарної хвороби, а також несприятливих серцево-судинних подій.
Співвідношення ліпопротеїнів
Співвідношення ліпопротеїнів є індикаторами серцево-судинного ризику, які мають більшу прогностичну силу, ніж відповідні ліпопротеїни, що розглядаються окремо. Регулярна оцінка цих співвідношень може надати точнішу інформацію щодо кардіометаболічного ризику пацієнтів.
Серед цих співвідношень виділяють співвідношення загальний холестерин / ЛПВЩ, відоме як атерогенний індекс, і співвідношення ЛПНЩ/ЛПВЩ. Останнє, схоже, має валідність, подібну до такої співвідношення загальний холестерин / ЛПВЩ, оскільки приблизно дві третини холестерину плазми міститься в ЛПНЩ, а отже, загальний холестерин і холестерин ЛПНЩ тісно пов’язані між собою [35].
Пацієнти з високими значеннями загального холестерину / ЛПВЩ або ЛПНЩ/ЛПВЩ мають більший серцево-судинний ризик через дисбаланс між холестерином, що транспортується атерогенними ліпопротеїнами, та холестерином, що транспортується захисними ліпопротеїнами. Це може бути пов’язано зі збільшенням проатерогенної фракції ліпопротеїнів у чисельнику, зменшенням антиатеросклеротичної фракції в знаменнику або з обома варіантами [36].
В огляді J. Millan і співавт. розглянуто декілька досліджень, які демонструють перевагу цих співвідношень ліпопротеїнів у прогнозуванні коронарних подій і тяжкості ІХС порівняно з ізольованими значеннями холестерину, ЛПНЩ та ЛПВЩ. Зокрема, значення 5,5 для співвідношення холестерину ЛПВЩ асоціюється з помірним серцево-судинним ризиком, тоді як пацієнти зі співвідношенням ЛПНЩ/ЛПВЩ >5 мають ризик коронарних подій у 6 разів вищий, аніж ті, що мають значення <5 [37].
Варто згадати про холестерин не-ЛПВЩ, який включає холестерин, що міститься в усіх атерогенних ліпопротеїнах (ЛПНЩ, ліпопротеїн (а), ЛПДНЩ, ЛППЩ, хіломікрони та їхні залишки). Цей специфічний тип холестерину був запропонований як вторинна терапевтична мішень для осіб із підвищеним рівнем ТГ, а також розглядався як потенційний сурогатний маркер концентрації аполіпопротеїну В у сироватці крові. Оптимальним вважається рівень холестерину не-ЛПВЩ <130 мг/дл. Вищий за цей поріг рівень пов’язаний із підвищеним ризиком серцево-судинних ускладнень [38]. Відштовхуючись від рівня холестерину не-ЛПВЩ, можна розрахувати співвідношення холестерину не-ЛПВЩ / ЛПВЩ. Хоча в небагатьох дослідженнях оцінювали достовірність цього співвідношення ліпопротеїнів у прогнозуванні серцево-судинних захворювань, схоже, що воно має прогностичну силу, подібну до такої співвідношення загального холестерину / ЛПВЩ, на основі якого було отримано співвідношення ЛПНЩ/ЛПВЩ [39].
Останнє співвідношення, здатне прогнозувати серцево-судинний ризик, – це співвідношення між ТГ і холестерином ЛПВЩ (ТГ/ЛПВЩ), використане P.L. Luz і співавт. Вони виміряли значення цього співвідношення в 374 пацієнтів із високим серцево-судинним ризиком, які проходили коронарну ангіографію з підозрою на ІХС, і продемонстрували, що цей показник сильно корелює зі ступенем і тяжкістю ураження коронарних судин, причому цей зв’язок виявився вищим, аніж між окремими показниками ліпопротеїнів [40]. Зокрема, співвідношення ТГ/ЛПВЩ >4 є сильним незалежним предиктором розвитку ІХС і мікросудинної дисфункції [41].
Аполіпопротеїн В та холестерин не-ЛПВЩ
Johannesen і співавт. провели дослідження, котре показало, що в пацієнтів, які проходять лікування статинами, підвищені рівні аполіпопротеїну В і холестерину не-ЛПВЩ, а не холестерину ЛПНЩ, корелюють із ЗР смертності від усіх причин та інфаркту міокарда. Аналіз розбіжностей показав, що аполіпопротеїн В слугує точнішим маркером ризику смертності від усіх причин у пацієнтів, які отримують лікування статинами, порівняно з холестерином ЛПНЩ або не-ЛПВЩ. Окрім того, аполіпопротеїн В був визначений як точніший маркер ризику інфаркту міокарда, ніж холестерин ЛПНЩ [42].
Обговорення
Аналіз співвідношення загального холестерину / ЛПВЩ, ЛПНЩ/ЛПВЩ, ТГ/ЛПВЩ і не-ЛПВЩ/ЛПВЩ обґрунтований результатами багатьох досліджень, які показали, що ці співвідношення є показниками серцево-судинного ризику з вищою прогностичною силою, ніж у відповідних ліпопротеїнів, які розглядаються окремо. Співвідношення загального холестерину / ЛПВЩ, відоме як атерогенний індекс, і співвідношення ЛПНЩ/ЛПВЩ, схоже, перекривають одне одного, оскільки приблизно дві третини холестерину в плазмі міститься в ЛПНЩ. У письмовому огляді J. Millan і співавт. чітко зазначено, що значення загального холестерину / ЛПВЩ ≥5,5 і ЛПНЩ/ЛПВЩ >5 асоціюються з підвищеним ризиком коронарних подій [37].
Що стосується СТЛ, то Zhou та співавт. спостерігали пацієнтів з інфарктом міокарда з підйомом сегмента ST і значенням СТЛ >171 [43] (табл.).
|
Таблиця. Пороги нових чинників серцево-судинного ризику |
|
|
Новий чинник серцево-судинного ризику |
Поріг |
|
Ліпопротеїн (а) |
50 мг/дл |
|
Загальний холестерин |
43 мг/дл |
|
Співвідношення моноцитів/ЛПВЩ |
17,5 |
|
Співвідношення тромбоцитів/лімфоцитів |
171 |
|
Співвідношення ЛПНЩ/ЛПВЩ |
5 |
|
Співвідношення ТГ/ЛПВЩ |
4 |
Можливу роль у залишковому серцево-судинному ризику може відігравати коронарна мікросудинна дисфункція, котра є поширеним станом, що створює значні проблеми для кардіологів через свою інвалідизувальну природу, часто проявляючись у вигляді стійкої стенокардії в уражених пацієнтів [44]. Серед осіб, особливо жінок, які проходять коронарну ангіографію для оцінювання болю в грудній клітці та стабільної стенокардії, значна частина (20-30%) мають нормальні показники коронарних ангіограм. Цей специфічний прояв називають первинною мікросудинною стенокардією (МСС), щоб відрізнити її від інших форм МСС, пов’язаних із захворюваннями, які можна ідентифікувати [45]. При первинній МСС дисфункція насамперед уражає преартеріоли, причому порушення функції ендотелію є ключовою ознакою.
Останніми роками значні наукові зусилля були спрямовані на характеристику МСС і з’ясування її патологічних механізмів. Етіологія МСС, імовірно, включає численні механізми, проте, незважаючи на досягнутий прогрес, багато аспектів патогенезу залишаються нез’ясованими. Відносна важливість різних чинників ризику та нові зміни функції ендотелію при МСС є сферами постійних досліджень [46].
За матеріалами: Sucato V., Comparato F., Ortello A., Galassi A.R., Novo G. Residual cardiovascular risk: role of remnants cholesterol, monocyte/HDL ratio and lipoprotein ratios on personalized cardiovascular prevention. J. Pers. Med. 2024; 14: 460. https://doi.org/10.3390/jpm14050460.
Реферативний огляд підготувала Дарія Чорна
Медична газета «Здоров’я України 21 сторіччя» № 15 (576), 2024 р



