29 жовтня, 2024
Oмепразол та інші зірки в сузір’ї інгібіторів протонної помпи: окремі питання безпеки і міжлікарських взаємодій
Більшість має певний світогляд, який визначила меншість.
Станіслав Єжи Лец
 Використання інгібіторів протонної помпи (ІПП), цих потужних антагоністів секреції шлункової кислоти, для лікування кислотно-пов’язаних розладів, таких як гастроезофагеальна рефлюксна хвороба та виразкова хвороба, а також для профілактики гастродуоденальних уражень у пацієнтів, які приймають ацетилсаліцилову кислоту (АСК) або нестероїдні протизапальні препарати (НПЗП), швидко зросло протягом останніх десятиліть.
Використання інгібіторів протонної помпи (ІПП), цих потужних антагоністів секреції шлункової кислоти, для лікування кислотно-пов’язаних розладів, таких як гастроезофагеальна рефлюксна хвороба та виразкова хвороба, а також для профілактики гастродуоденальних уражень у пацієнтів, які приймають ацетилсаліцилову кислоту (АСК) або нестероїдні протизапальні препарати (НПЗП), швидко зросло протягом останніх десятиліть.
Наразі ІПП є одним із найпризначуваніших класів лікарських засобів у світі. Водночас у питанні співвідношення ризику та користі застосування ІПП, зокрема при антитромботичній терапії, досі залишаються певні суперечності. Сучасні клінічні й безпекові дані доводять актуальність застосування омепразолу.
Нині важко повірити, що відносно нещодавно, на початку ХХ століття, лікування виразкової та гастроезофагеальної рефлюксної хвороби (ГЕРХ) полягало в призначенні лужних продуктів харчування: молока, яєць, пюре. Дещо пізніше першу скрипку в терапії цих захворювань стала грати питна сода – вона полегшувала стан хворих, але, на жаль, не запобігала розвитку ускладнень. У середині ХХ століття з’явилися холіноблокатори, і на сцену вийшов атропін, який частково інгібував продукцію соляної кислоти за допомогою блокади мускаринових рецепторів парієтальних клітин. Незначна ефективність, численні побічні ефекти не дозволили атропіну тривалий час утримувати лідерські позиції в лікуванні кислотозалежних захворювань (КЗЗ), і йому на зміну прийшли блокатори Н2-рецепторів.
Настав час ранітидину та фамотидину – вони внесли істотні зміни до усталених принципів лікування КЗЗ: механізм дії цих препаратів полягав у блокуванні гістамінових рецепторів у парієтальних клітинах, що супроводжувалося досягненням нетривалого контролю за синтезом соляної кислоти.
Попри вищу ефективність порівняно з М-холіноблокаторами, застосування Н2-блокаторів рідко забезпечувало повне відновлення та загоєння дефектів слизової оболонки через нездатність цих препаратів тривало блокувати секрецію соляної кислоти та довго утримувати цільовий рН.
І ось нарешті на небосхилі з’явилася нова зірка – омепразол, представник раніше невідомої групи лікарських засобів, а саме ІПП. Ефект, спричинений появою омепразолу, часто порівнюють із масштабною терапевтичною революцією: висока афінність до протонної помпи парієтальних клітин шлунка та сприятливіший порівняно з попередниками профіль побічних дій перевернули уявлення про лікування КЗЗ, які панували до того. Роки широкомасштабного клінічного застосування, безліч порівняльних клінічних досліджень переконливо підтвердили перевагу першого представника класу ІПП над Н2-блокаторами. Така переконлива перемога омепразолу в лікуванні виразкової хвороби та ГЕРХ створила передумови для синтезу інших ІПП. І невдовзі сімейство ІПП поповнилося новими членами – лансопразол, пантопразол, рабепразол, езомепразол приєдналися до свого родоначальника в боротьбі з КЗЗ. Кількість призначень ІПП швидко зросла: лише протягом 8 років (з 2000-го по 2008-й) частота застосування ІПП збільшилася на 200,8%, натомість кількість призначень Н2-блокаторів значно скоротилася. Ось так, поступово, з появою нових препаратів і сучасних знань змінювалися світогляд, стандарти та підходи до лікування КЗЗ.
Трохи фармакології
ІПП, потрапляючи в організм у неактивному вигляді проліків, активуються виключно в суперкислому середовищі (за рівня рН 1,0-2,0). Короткочасність, незворотність і вибірковість дії ІПП дозволяють швидко та надійно вивести з ладу активовані протонні насоси. Відновлення синтезу соляної кислоти можливе лише через певний проміжок часу, необхідний для синтезу нових білкових молекул, які входять до складу протонної помпи. ІПП – препарати, які «живуть» дуже недовго (період напіввиведення – 0,5-2 год), – здатні забезпечити надзвичайно тривалий кислотосупресивний ефект при одноразовому прийомі протягом доби. Нині ІПП продовжують міцно утримувати пальму першості серед усіх наявних класів антисекреторних лікарських засобів: вони здатні утримувати рН у шлунку ≥4,0 протягом 18 год упродовж доби. Після прийому стандартної дози ІПП синтез соляної кислоти повністю відновлюється лише через 72-96 год, а біодоступність препаратів зростає з прийомом кожної наступної дози. Короткий період напіввиведення ІПП забезпечує низьку токсичність препаратів цієї групи навіть у хворих похилого віку або пацієнтів із нирковою/печінковою недостатністю. Лише у випадках вираженої печінкової недостатності може знадобитися зменшення дози цих препаратів.
На відміну від ІПП, Н2-блокатори починають діяти значно швидше, однак їх прийом супроводжується розвитком тахіфілаксії, а антисекреторна активність знижується вже через 12-24 год після прийому. Наразі Н2-блокатори використовуються досить рідко і призначаються для лікування вкрай обмеженого переліку захворювань (легка неерозивна ГЕРХ, легкий перебіг функціональної диспепсії, гіперчутливість до ІПП), натомість спектр застосування ІПП значно ширший (табл. 1).
|
Таблиця 1. Області застосування ІПП |
|
• ГЕРХ |
|
• Стравохід Баррета, пептичні стриктури стравоходу |
|
• Еозинофільний езофагіт |
|
• Необстежена та функціональна диспепсія |
|
• Пептична виразкова хвороба шлунка та дванадцятипалої кишки |
|
• Ерадикація Helicobacter pylori |
|
• Синдром Золлінгера-Еллісона |
|
• Профілактика НПЗП-гастропатії, стресової виразки |
|
• Кровотеча з верхніх відділів шлунково-кишкового тракту |
|
• Екзокринна недостатність підшлункової залози |
У настанові Європейського товариства кардіологів (European Society of Cardiology, ESC) щодо лікування гострого коронарного синдрому (ГКС) наводиться ще одне показання для призначення ІПП при подвійній антитромбоцитарній терапії (ПАТТ) (ESC, 2023) (табл. 2).
|
Таблиця 2. Рекомендації ESC (2023) щодо призначення ІПП при ПАТТ (при ГКС) |
|
Комбінація ІПП із подвійною антитромбоцитарною терапією (ПАТТ) рекомендована пацієнтам із високим ризиком розвитку гастроінтестинальної кровотечі (обтяжений анамнез через виразкову хворобу та шлунково-кишкові кровотечі, прийом антикоагулянтів, тривале застосування НПЗП/кортикостероїдів) або за наявності ≥2 із зазначених далі факторів: вік ≥65 років, диспепсія, ГЕРХ, інфікування Helicobacter pylori, хронічне зловживання алкоголем. |
Завзяті змагання, запеклі суперечки та несподіваний парадокс
Ситуацію рівності та братерства в сімействі ІПП порушило бажання учнів перевершити вчителя: хтось здавався сильнішим, хтось – швидшим, а хтось – тривалішим. Однак вираженість кислотосупресивної дії виявилася зіставною з такою решти ІПП, а за тривалістю підтримання внутрішньошлункового рН ≈4 омепразол (11,8 год), хоча й поступався езомепразолу (14 год) та рабепразолу (12 год), але перевершував лансопразол (11,5 год) і пантопразол (10,1 год) (Miner et al., 2003). Доведено, що використання омепразолу у хворих, які приймають ПАТТ із включенням низьких доз АСК, запобігає пошкодженню слизової оболонки верхніх відділів шлунково-кишкового тракту (ШКТ) і зменшує ризик кровотеч (Дорофєєв А.Е., 2017). Вивчення механізмів дії омепразолу дозволило встановити, що, крім значного зниження секреції соляної кислоти, під впливом цього препарату достовірно збільшується експресія гена Bcl‑2 та синтез протеїну Ki‑67 у хворих на НПЗП-асоційовані виразки, ускладнені кровотечею. Саме завдяки цим властивостям обмежується активність апоптозу та стимулюється проліферація епітелію ШКТ, прискорюється репарація ерозивно-виразкових уражень, спричинених прийомом НПЗП (Rantanen T. et al., 2014).
Утім, найзапекліші суперечки про перевагу одного ІПП над іншими виникли на ґрунті безпеки їх застосування в окремої групи хворих – у пацієнтів, які отримують ПАТТ за допомогою ацетилсаліцилової кислоти (АСК) та інгібітора P2Y12 клопідогреля. У ході спостережних досліджень, які вивчали можливі взаємодії при одночасному прийомі ІПП та клопідогрелю, було отримано неоднозначні результати: деякі свідчили про погіршення серцево-судинних наслідків, інші не підтверджували наявність такого зв’язку. Ретельний аналіз можливих несприятливих наслідків поєднаного застосування ІПП та інгібітора P2Y12 показав, що можлива причина їх виникнення полягає в особливостях метаболізму зазначених медикаментів. Виявилося, що метаболізм цих препаратів відбувається в печінці за участю переважно трьох ізоферментів системи цитохрому Р450: CYP2C19, CYP2C9, CYP3A4. Висловлено припущення, що ІПП, вступаючи у взаємодію із зазначеними ферментами, в такий спосіб інгібують перетворення клопідогрелю на його активний метаболіт, знижуючи ефективність останнього й опосередковано посилюючи агрегацію тромбоцитів. На перший погляд, все виявилося досить просто: клопідогрель метаболізується за допомогою CYP2С19, отже, за необхідності одночасного прийому клопідогрелю та ІПП необхідно використовувати такий кислотосупресивний препарат, який не впливав би на цей ізофермент.
Управління з контролю продуктів харчування та лікарських засобів США (FDA, 2009) не забарилося опублікувати застереження щодо того, що небажано застосовувати клопідогрель та ІПП, особливо омепразол й езомепразол (найбільш вивчені представники цього класу лікарських засобів на той час), та рекомендувало до застосування менш вивчений препарат пантопразол, який, імовірно, не впливав на CYP2С19.
Активне клінічне застосування пантопразолу, а також ретельне вивчення властивостей інших ІПП змусило експертів засумніватися в правильності таких висновків. Виявилося, що метаболізм клопідогрелю відбувається не лише за рахунок CYP2С19, а й за допомогою CYP2С9, CYP3А4, а різні представники групи ІПП чинять різний вплив на метаболізм системи цитохрому Р450. Тому вплив ІПП на метаболізм клопідогрелю та подальші серцево-судинні наслідки можуть суттєво відрізнятися.
Три нищівні удари по усталеному стереотипу
Незабаром з’явилися результати клінічних досліджень і метааналізів. Першого нищівного удару, який похитнув усталений стереотип щодо здатності омепразолу збільшувати серцево-судинний ризик у хворих, котрі отримують ПАТТ, завдало дослідження COGENT (Clopidogrel and the Optimization of Gastrointestinal Events Trial, 2010). Це міжнародне рандомізоване подвійне сліпе контрольоване за допомогою двох плацебо паралельне групове дослідження (n=3873) ефективності й безпеки фіксованої комбінації клопідогрелю (75 мг) та омепразолу (20 мг) порівняно з монотерапією клопідогрелем дало неочікувані результати (всі пацієнти в цьому дослідженні додатково приймали АСК). Упродовж усього періоду спостереження, тривалість якого становила 180 днів, ураження ШКТ (явна/прихована кровотеча, симптоматичні гастродуоденальні виразки/ерозії, обструкція, перфорація) було зафіксовано в 51 пацієнта, при цьому зазначені стани достовірно рідше виникали у хворих, які отримували омепразол (1,1%), порівняно з учасниками, котрі приймали плацебо (2,9%; відношення ризиків (ВР) для омепразолу 0,34; 95% довірчий інтервал (ДІ) 0,18-0,63; р=0,001). Поряд із цим частота виникнення нефатального інфаркту міокарда, інсульту, реваскуляризації, летального наслідку з кардіоваскулярних причин достовірно не відрізнялася в групах омепразолу (4,9%) та плацебо (5,7%; ВР 0,99; 95% ДІ 0,68-1,44; р=0,96). Опублікувавши отримані дані (табл. 3, рис. 1), автори дослідження резюмували, що не зафіксовано значущих кардіоваскулярних взаємодій між клопідогрелем та омепразолом, проте ці результати не дозволяють цілком виключити клінічно значущі відмінності в кардіоваскулярних подіях, зумовлених застосуванням ІПП (табл. 3).
|
Таблиця 3. Основні результати дослідження COGENT: безпека омепразолу порівняно з плацебо |
||
|
Подія |
ВР (95% ДІ) |
р |
|
Комбіновані гастроінтестинальні події |
0,34 (0,18-0,63) |
<0,001 |
|
Комбіновані кардіоваскулярні події |
0,99 (0,68-1,44) |
0,96 |
|
Інфаркт міокарда |
0,92 (0,44-1,90) |
0,81 |
|
Реваскуляризація |
0,91 (0,59-1,38) |
0,64 |
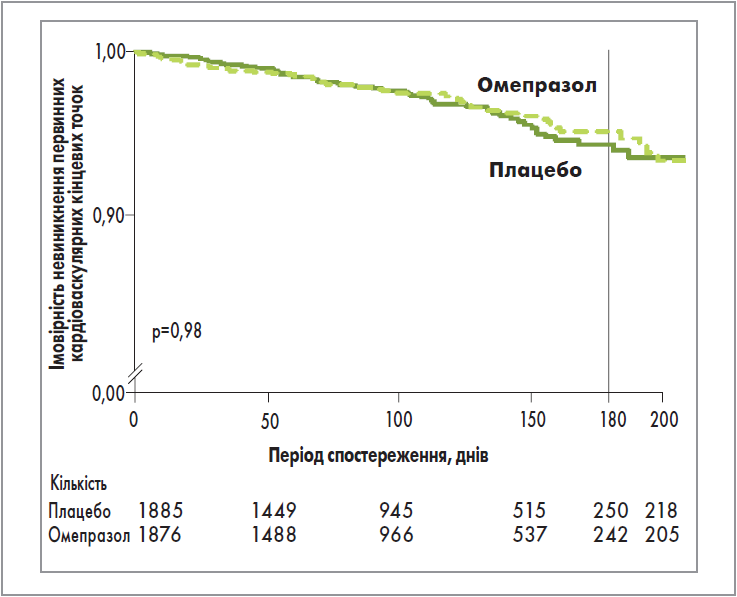 Рис. 1. Результати дослідження COGENT: розрахунок імовірності невиникнення первинних кардіоваскулярних подій за методом Каплана-Меєра (Bhatt D. et al., 2010)
Рис. 1. Результати дослідження COGENT: розрахунок імовірності невиникнення первинних кардіоваскулярних подій за методом Каплана-Меєра (Bhatt D. et al., 2010)
Сформульовані висновки були сприйняті медичною громадськістю з великою настороженістю – лише за рік перед цим FDA настійно рекомендувало застосування пантопразолу. Ще одним поясненням цього факту може стати дострокове завершення дослідження: відповідно до планів авторів проєкту, в зазначеному випробуванні мали взяти участь 5 тис. хворих, але повільний набір пацієнтів і невелика кількість кардіоваскулярних подій стали приводом припинити фінансування та закрити COGENT. Однак через 6 років результати цього дослідження було проаналізовано та перевірено ще раз іншою групою вчених, які не брали безпосередньої участі в його проведенні. М. Vaduganathan і співавт. (2016) повністю підтвердили висновки, сформульовані D. Bhatt і співавт.: у пацієнтів, які перенесли черезшкірне коронарне втручання (n=2676), омепразол значно зменшував імовірність розвитку гастроінтестинальних подій без суттєвого підвищення ризику кардіоваскулярних подій порівняно з плацебо (5,4 vs 6,3% відповідно; ВР 1,0; 95% ДІ 0,67-1,50; р=1,00). Аналогічно в когорті хворих із гострим коронарним синдромом (n=1573) омепразол запобігав виникненню значущих гастроінтестинальних подій, не провокуючи зростання ймовірності розвитку кардіоваскулярних подій порівняно з плацебо (5,6 vs 4,5% відповідно; ВР 1,4; 95% ДІ 0,77-2,53; р=0,27).
Другим, не менш серйозним, ударом по кардіологічному образу пантопразолу стала публікація в авторитетному журналі Американської кардіологічної асоціації систематичного огляду, підготовлена під керівництвом М. Sherwood (2015). Метааналіз 6 відібраних досліджень виявив підвищення ризику виникнення небажаних кардіоваскулярних подій у пацієнтів, які приймали пантопразол (ВР 1,38; 95% ДІ 1,12‑1,70), лансопразол (ВР 1,29; 95% ДІ 1,09-1, 52) або езомепразол (ВР 1,27; 95% ДІ 1,02-1,58) порівняно з хворими, які не отримували ІПП. Вчені особливо наголосили на тому, що згаданий зв’язок не був значущим для омепразолу (ВР 1,16; 95% ДІ 0,93-1,44), тобто омепразол може використовуватися при проведенні ПАТТ, тому що не чинить негативного впливу на серцево-судинний ризик (рис. 2).
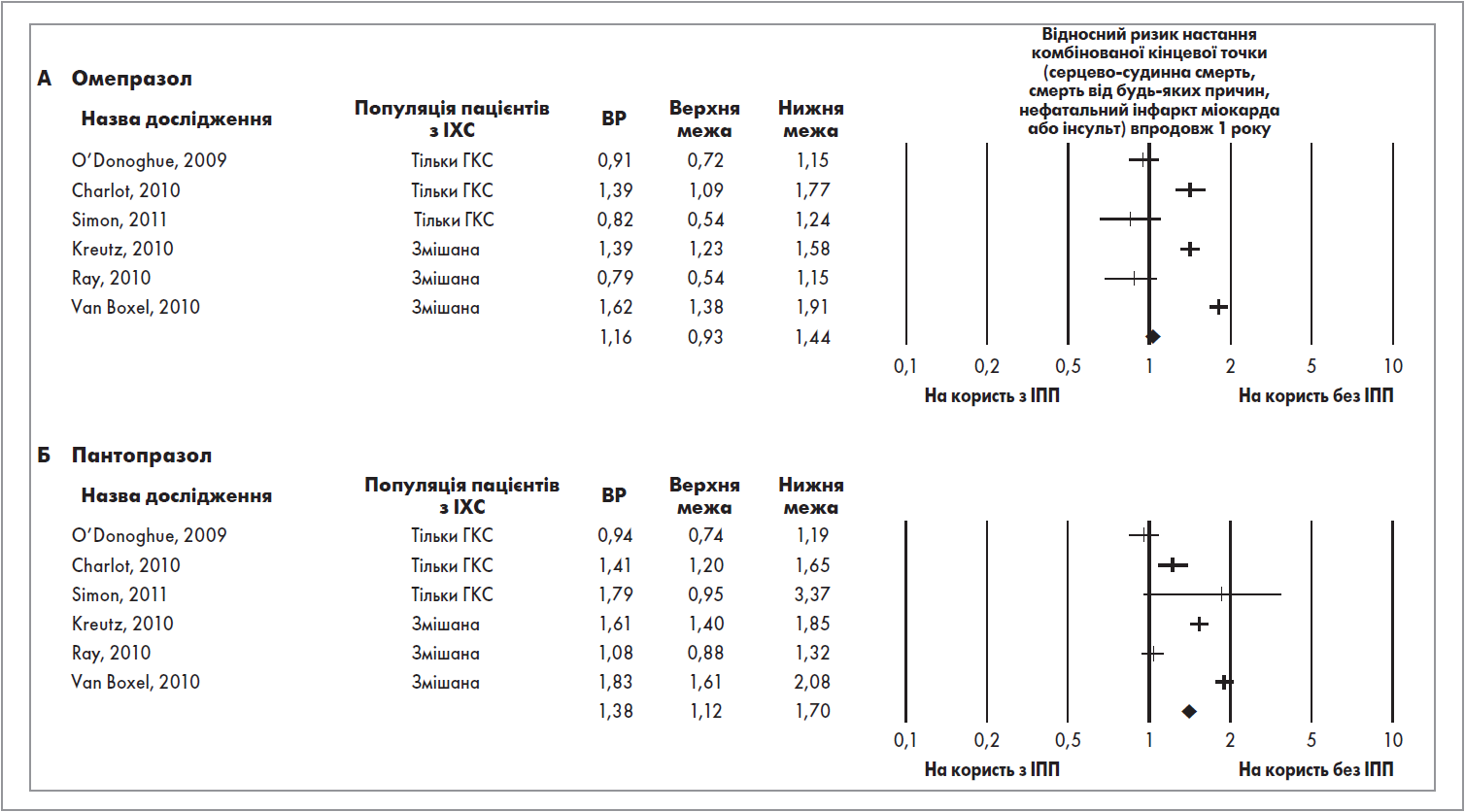 Рис. 2. Результати метааналізів поєднаного застосування деяких ІПП і клопідогрелю у пацієнтів з ішемічною хворобою серця (Sherwood М. et al., 2015): переконлива перевага омепразолу над пантопразолом
Рис. 2. Результати метааналізів поєднаного застосування деяких ІПП і клопідогрелю у пацієнтів з ішемічною хворобою серця (Sherwood М. et al., 2015): переконлива перевага омепразолу над пантопразолом
Примітки: ІХС – ішемічна хвороба серця; ГКС – гострий коронарний синдром.
Коментуючи отримані дані, М. Sherwood і співавт. висловили припущення, що аналіз показників щодо безпеки прийому ІПП при проведенні ПАТТ слід проводити для кожного представника цієї групи окремо, не узагальнюючи всі дані в одну групу та не розглядаючи питання з позиції «користь/шкода всіх ІПП».
Надзвичайно цікавими є результати обсерваційного дослідження, виконаного під керівництвом А. Guérin (2016). Дослідники спробували встановити, як вплинула рекомендація FDA щодо переваги призначення пантопразолу при проведенні ПАТТ. Вчені констатували два важливі факти: публікація рекомендації FDA призвела до зменшення загальної кількості пацієнтів, яким було призначено комбінацію клопідогрелю та ІПП; проте, незважаючи на зниження частки хворих, котрі отримували зазначену комбінацію, омепразол залишався найчастіше використовуваним препаратом, що призначається одночасно з клопідогрелем.
Третього удару завдали Т. Shamliyan і співавт. (2017), автори масштабної роботи, в основу якої лягли результати 17 систематичних оглядів і метааналізів, 16 рандомізованих контрольованих досліджень і 16 обсерваційних досліджень. Команда вчених проаналізувала особливості поєднаного прийому ІПП із 10 різними класами лікарських засобів. Вивчивши отримані дані, Т. Shamliyan і співавт. резюмували: «Щодо конкретних ІПП одночасний прийом пантопразолу або езомепразолу, але не омепразолу та лансопразолу, асоційований з підвищенням ризику загальної летальності, нефатального інфаркту міокарда та інсульту».
Цироз печінки та ІПП: усе зовсім непросто
Ще одним каменем спотикання в проблемі безпечного застосування ІПП став цироз печінки. Хворим на цироз печінки, незалежно від етіологічної причини захворювання, притаманний високий ризик розвитку портальної гіпертензивної гастропатії, появи вариксів у стравоході та шлунку, а також виникнення кровотечі з варикозно розширених вен. Для лікування та профілактики зазначених ускладнень використовуються ІПП. Однак виявилося, що ця проста на перший погляд рекомендація тягне за собою низку серйозних проблем: застосування ІПП у хворих на цироз печінки асоціюється зі стрімким зростанням ризику виникнення інфекційних ускладнень та печінкової енцефалопатії. Реакція медичної громадськості була миттєвою: одні вчені рекомендували значно обмежити показання до призначення ІПП у цій категорії хворих, інші висловили радикальнішу думку: вважати цироз печінки протипоказанням до призначення зазначених лікарських засобів.
Хмари, що згустилися над ІПП, розвіяла стаття R. Weersink і співавт., опублікована у квітні 2018 року в авторитетному журналі British Journal of Clinical Pharmacology. Ця група вчених дослухалася рекомендацій М. Sherwood і проаналізувала безпеку застосування ІПП, не поєднуючи всі препарати в одну групу. Ґрунтуючись на результатах аналізу 69 досліджень, автори метааналізу довели, що застосування лише трьох ІПП не асоційоване з появою «додаткових відомих ризиків». До цієї категорії увійшли омепразол, езомепразол і рабепразол. R. Weersink і співавт. встановили, що безпека прийому вищеназваних ІПП залежить від ступеня тяжкості цирозу, визначеної за шкалою Чайлда-П’ю: хворим на цироз печінки, стан яких відповідає класу А і В, можна призначати омепразол і рабепразол, але бажано зменшити максимальну добову дозу зазначених лікарських засобів. Пацієнтам, які перебувають у вкрай тяжкому стані (клас С), слід рекомендувати лише езомепразол у максимальній добовій дозі 20 мг. Пантопразол і лансопразол визнані «небезпечними препаратами», тому що їх прийом асоційований з 4-8-кратним збільшенням ризику різних ускладнень.
Підсумки, або Далі буде?
Наразі питання безпеки одночасного застосування ІПП і клопідогрелю в складі ПАТТ залишається відкритим. На думку провідних міжнародних експертів, слід очікувати на оновлення рекомендацій різних кардіологічних товариств щодо вибору ІПП при проведенні ПАТТ.
Ремарка. Омез®
Серед багатьох генеричних омепразолів, представлених на вітчизняному фармацевтичному ринку, популярністю користується препарат Омез®, який представляє компанія Dr. Reddy’s Laboratories Ltd. У послужному списку Омезу – клінічний досвід його активного застосування в багатьох країнах світу, рівний декільком десятиліттям. За цей час Омез® встиг довести свою терапевтичну еквівалентність оригінальному омепразолу. Небрендований омепразол виробництва Dr. Reddy’s Laboratories Ltd. посів гідне місце у відомій Orange Book, яка публікується FDA. Застосування Омезу обговорювалося міжнародною експертною групою Gastrosphere 1.0 та 2.0 для профілактики і лікування НПЗП-індукованих уражень верхніх відділів ШКТ. Омез® у дозі 10-20 мг може використовуватися для проведення безпечної кислотосупресивної терапії у хворих на цироз печінки класу А-В за шкалою Чайлда-П’ю.
Висновки
На підставі вищевикладеного можна стверджувати, що нині омепразол є одним із найбільш вивчених препаратів у своєму класі. Важливо також відзначити, що омепразол є одним із найчастіше призначуваних ІПП і як ІПП входить до стандартів лікування КЗЗ у США та країнах Європи. На українському фармацевтичному ринку серед генеричних омепразолів популярність має Омез®.
Список літератури знаходиться в редакції.
Стаття підготовлена за підтримки компанії «Др. Редді’с Лабораторіз» для надання професійної інформації спеціалістам у сфері охорони здоров’я. Містить інформацію про лікарський засіб (інформація про який також наведена в супутньому інфоблоці, див.).
ОМЕ-26-06-2024-Rx1-7.4
Медична газета «Здоров’я України 21 сторіччя» № 18 (579), 2024 р



 Ткач С.М.
Ткач С.М.
