9 квітня, 2023
Мікробіологічний пейзаж та антибіотикотерапія при мінно-вибуховій травмі

За матеріалами конференції
У статті розглянуто сучасні принципи профілактики й лікування інфекційних ускладнень при бойовій травмі. Проаналізовано проблему нераціонального використання антибактеріальних препаратів в умовах зростання резистентності збудників.
Ключові слова: мінно-вибухова травма, інфекційні ускладнення, антибіотикотерапія, профілактика, цефоперазон/сульбактам.
Мінно-вибухова травма – це поєднана травма, що виникає у результаті імпульсного впливу комплексу вражаючих факторів мінно-вибухового боєприпасу. Мінно-вибухові ураження є одними з найбільш тяжких та специфічних видів травм. Частота медико-санітарних втрат під час бойових дій внаслідок мінно-вибухової травми сягає 25% (Гур’єв С.О. та співавт., 2015). Такі травми, як і вогнепальні поранення, завжди є первинно мікробно забрудненими, що вимагає від медичного персоналу усвідомлення важливості вчасного й раціонального застосування антибактеріальної терапії у постраждалих пацієнтів.
Цю актуальну тему висвітлив на 14-му Британо-українському симпозіумі «Актуальні питання менеджменту травми» завідувач кафедри анестезіології та інтенсивної терапії Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), доктор медичних наук, професор Олег Анатолійович Лоскутов у доповіді «Мікробіологічний пейзаж та антибіотикотерапія при мінно-вибуховій травмі».
 Насамперед спікер зазначив, що актуальність застосування антибіотикотерапії при вогнепальних пораненнях та мінно-вибухових травмах є беззаперечною. Адже дані, отримані з театру бойових дій в Іраку та Афганістані, показали, що серед постраждалих із мінно-вибуховими травмами 27% осіб перенесли хоча б одне інфекційне ускладнення. У 16% пацієнтів із пораненням живота рани ускладнювалися сепсисом. Ураження грудної клітки у 23% випадків були пов’язані з інфекційними ускладненнями, а у постраждалих із відкритими переломами кінцівок приблизно у 15% випадків розвинувся остеомієліт (Conger N.G. et al., 2008; Yan H.C. et al., 2014).
Насамперед спікер зазначив, що актуальність застосування антибіотикотерапії при вогнепальних пораненнях та мінно-вибухових травмах є беззаперечною. Адже дані, отримані з театру бойових дій в Іраку та Афганістані, показали, що серед постраждалих із мінно-вибуховими травмами 27% осіб перенесли хоча б одне інфекційне ускладнення. У 16% пацієнтів із пораненням живота рани ускладнювалися сепсисом. Ураження грудної клітки у 23% випадків були пов’язані з інфекційними ускладненнями, а у постраждалих із відкритими переломами кінцівок приблизно у 15% випадків розвинувся остеомієліт (Conger N.G. et al., 2008; Yan H.C. et al., 2014).
Усі мінно-вибухові травми мають первинне мікробне забруднення, тому вкрай важливим і складним завданням для лікаря є правильний вибір антибактеріального препарату з метою запобігання розвитку інфекційних ускладнень. За даними L. Stewart et al. (2020), понад 50% уламків при мінно-вибуховій травмі залишаються не видаленими з рани. Крім того, багаторазові переливання компонентів крові після таких поранень призводять до повного обмінного переливання та втрати циркулюючих імунних тіл. Ці порушення регуляції можуть спричиняти розвиток синдрому системної запальної відповіді, який, імітуючи інфекцію, ускладнює діагностику й призводить до неадекватного призначення антибіотиків. Тому статистика використання антибіотиків, за даними одноцентрового огляду бойових травм, отриманих в Іраку, виглядає так: 23% травм були асоційовані з інфекцією, при цьому 10% поранених отримували у період госпіталізації один антибіотик, 18% – два антибіотики, 25% – три, 20% – чотири, а 26% таких пацієнтів– щонайменше п’ять антибіотиків (Stewart L. et al., 2020). Автори дослідження зазначають, що 36% поранених отримувати антибактеріальну терапію до виявлення зараження, причому 28% із них – більш ніж два препарати. Протягом тижня після виявлення інфекції 78% пацієнтів призначали лікування новим препаратом, притому що 71% із них отримували більше двох антибіотиків. У разі глибокого ураження м’яких тканин поранені зазвичай отримували два-три антибіотики, серед яких переважали комбінації різних груп антибактеріальних препаратів – карбапенемів, фторхінолонів і ванкоміцину.
Професор О.А. Лоскутов наголосив, що з кожним наступним воєнним конфліктом долати ранову інфекцію ставатиме все складніше, адже через нераціональне використання антибактеріальних препаратів зростає резистентність до них збудників (Sahli Z.T. et al., 2016). Так, невдовзі після початку бойових дій у ході операції «Іракська свобода» військові медики відзначали велику кількість мікроорганізмів із множинною лікарською стійкістю. Найбільш помітними з них були Acinetobacter baumannii, Pseudomonas aeruginosa, Klebsiella pneumoniae, метицилін-резистентний Staphylococcus aureus (MRSA). Примітно, що коли театр бойових дій перемістився з Іраку до Афганістану, мікробіологічний пейзаж ран також змінився: почали переважати бактерії – продуценти β-лактамаз (Escherichia coli, Enterobacter spp., K. pneumoniae) (Yan H.C. et al., 2017). Аналіз останнього збройного конфлікту в Афганістані показав, що при мікробіологічному дослідженні ран кінцівок у флорі переважали грамнегативні бактерії. Крім того, при полімікробних інфекціях у 61% пацієнтів виявлялися тільки бактерії, а у 30% – бактерії та гриби. Множинна лікарська стійкість спостерігалася у 32% ізолятів. Приблизно 52% колонізованих ран мали ≥1 мікроорганізм в одного й того ж пацієнта (Mende K. et al., 2019).
Спікер наголосив, що спектр домінуючих патогенів змінюється із часом і різниться залежно від розташування театру бойових дій, тому неможливо визначити єдиний стандартний режим антибактеріальної терапії, який був би доцільним у всіх таких поранених у майбутньому(Yan H.C. et al., 2017).
Антибактеріальна терапія мінно-вибухової травми
На сьогодні актуальними є рекомендації, викладені в американському керівництві «Emergency War Surgery» (2021), які вказують, що за неможливості проведення бактеріологічного дослідження емпірична антибіотикотерапія має тривати 7-10 днів. Призначення карбапенемів рекомендоване лише при пораненнях органів черевної порожнини та як альтернатива цефалоспоринам за неможливості їх застосування. Як основний препарат при емпіричному призначенні антибактеріальної терапії у більшості випадків застосовують цефазолін, а при значному забрудненні рани або приєднанні поранення органів черевної порожнини необхідно додати метронідазол.
Досвід українських колег (Криштафор Д.А. та співавт., 2015) щодо верифікації мікроорганізмів при бойовій травмі продемонстрував, що на 3-тю добу в мікрофлорі рани переважали умовно-патогенні мікроорганізми: E. coli, Staphylococcus haemolyticus, Proteus mirabilis. До 7-ї доби відбувалася контамінація рани госпітальною флорою на фоні успішної елімінації вихідної флори: А. bаumanii, P. aeruginosa, S. haemolyticus. На 10-ту добу, незважаючи на антибіотикотерапію, госпітальна флора продовжувала зростати й у переважної більшості поранених виявляли А. baumanii, P. aeruginosa. При цьому 21,3% висіяних збудників були чутливими до цефоперазону/сульбактаму і лише 10,6% – до карбапенемів. Крім того, висіяна А. baumanii виявляла стійку резистентність до карбапенемів, а P. aeruginosa виявляла чутливість лише в 10% випадків, причому чутливість до цефоперазону/сульбактаму становила 40 і 70% відповідно.
Гепацеф Комбі є комбінацією сульбактаму натрію та цефоперазону натрію. Сульбактам натрію, похідне основного пеніцилінового ядра, є незворотним інгібітором β-лактамази. Цефоперазон натрію – це напівсинтетичний цефалоспориновий антибіотик ІІІ покоління, який діє шляхом пригнічення біосинтезу мукопептиду клітинної стінки бактерій. Комбінована дія сульбактаму та цефоперазону є ефективною проти всіх мікроорганізмів, чутливих до цефоперазону. Крім того, доведено синергізм цефоперазону/сульбактаму (зниження мінімальних концентрацій комбінації, що пригнічують мікроорганізми, приблизно у 4 рази порівняно з такими концентраціями кожного компонента окремо) проти різних мікроорганізмів із найбільшою стійкістю, а саме: Haemophilus influenzae, види Bacteroides, види Staphylococcus, Acinetobacter calcoaceticus, Enterobacter aerogenes, E. coli, P. mirabilis, K. pneumoniae, Morganella morganii, Citrobacter freundii, Enterobacter cloacae, Citrobacter diversus.
Отже, препарат Гепацеф Комбі, порошок для розчину для ін’єкцій по 1,0/1,0 г по 2,0 г у флаконі, виробництва АТ «Київмедпрепарат», може бути застосований при мінно-вибухових травмах, якщо підтверджена чутливість до нього висіяного збудника.
Профілактика інфекційних ускладнень
Спікер навів основні положення рекомендацій O. Saeed et al. (2018) щодо профілактики інфекційних ускладнень при бойових травмах.
Стандартні заходи:
• гігієна рук (за настановами Всесвітньої організації охорони здоров’я):
– використання води з милом або дезінфікуючого засобу на спиртовій основі перед контактом із пацієнтом;
– використання води з милом або дезінфікуючого засобу на спиртовій основі перед асептичними процедурами;
– використання води з милом або дезінфікуючого засобу на спиртовій основі перед контактом із біологічними рідинами;
– використання води з милом або дезінфікуючого засобу на спиртовій основі після контакту із хворим;
– використання води з милом або дезінфікуючого засобу на спиртовій основі після контакту з оточенням пацієнта, навіть якщо були використані рукавички;
• використання ізолюючих халатів;
• використання захисних масок;
• використання захисних окулярів або лицьових щитків;
• щоденна обробка пацієнтів хлоргексидином у відділенні інтенсивної терапії (сприяє зниженню інфекцій, спричинених ванкоміцин-резистентними ентерококами та MRSA).
Специфічні заходи:
- використання локальної антибіотикограми для призначення емпіричної терапії;
- проведення постійної оцінки ран на наявність інфекції (посіви);
- використання максимально коротких курсів антибіотикотерапії при поширених інфекційних захворюваннях;
- використання цефалоспоринів протягом щонайменше 3 днів після травми для запобігання рановій інфекції при відкритих переломах;
- використання захищених цефалоспоринів при травмах живота; при розвитку шоку у таких пацієнтів рекомендоване введення ертапенему на госпітальному етапі;
- показане введення метронідазолу внутрішньовенно кожні 8-12 год при проникаючих пораненнях живота і грудної клітки, які призвели до ураження стравоходу;
- при інфекціях, стійких до β-лактамних антибіотиків, комбінація інгібіторів β-лактамаз (наприклад, сульбактам, клавуланова кислота й тазобактам) із β-лактамними антибіотиками допомагає посилити ефективність останніх;
- кількість бактерій збільшується в геометричній прогресії з моменту травми, а перші 6 год після поранення є основним періодом контамінації. Необхідно збільшити час лікування антибіотиками, якщо неминуча затримка у їх введенні при відкритій травмі;
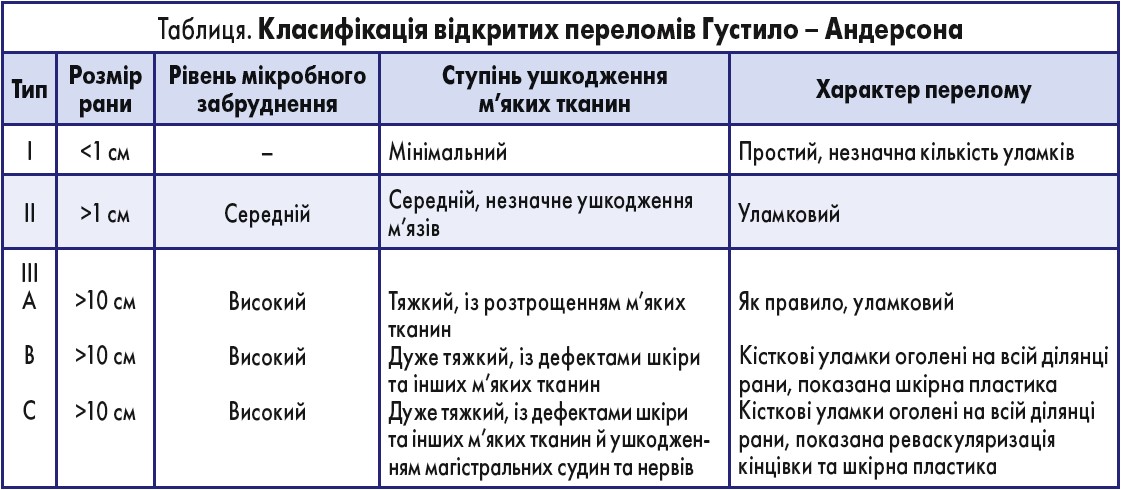
- призначення антибіотиків широкого спектра дії внутрішньовенно має базуватися на класифікації Густило – Андерсона (таблиця);
- введення повторної дози протимікробних препаратів необхідне у разі великої крововтрати (1500-2000 мл);
- профілактика гепатиту С не рекомендована, але при проникаючому пораненні вибуховою хвилею через 2, 4 та 6 міс можна розглянути питання про проведення тестування;
- у закладах другого й третього рівнів надання медичної допомоги має бути призначений співробітник із профілактики та контролю інфекцій як штатна посада.
Впровадження сучасних принципів профілактики й лікування інфекційних ускладнень бойової травми на сьогодні є вкрай актуальним завданням і має базуватися на проведенні мікробіологічного моніторингу. Правильне призначення антибактеріального препарату при мінно-вибухових травмах дозволяє запобігти розвитку інфекційних ускладнень.
Підготувала Марія Грицуля
Тематичний номер «Хірургія. Ортопедія. Травматологія. Інтенсивна терапія» № 5 (52), 2022 р.