19 квітня, 2025
Деякі периферичні причини запаморочення: перебіг, діагностика й лікування
 Восени минулого року відбувся цикл майстер-класів у онлайн-форматі «Мультидисциплінарний підхід до проблемних питань неврології та психіатрії: нові стратегії лікування». На одній із зустрічей розглядалися гострі й невідкладні стани у психіатрії та неврології. Про деякі периферичні причини запаморочення – їх характеристики й перебіг, а також особливості діагностики та лікування – розповів Михайло Михайлович Орос, д.мед.н., професор, завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Восени минулого року відбувся цикл майстер-класів у онлайн-форматі «Мультидисциплінарний підхід до проблемних питань неврології та психіатрії: нові стратегії лікування». На одній із зустрічей розглядалися гострі й невідкладні стани у психіатрії та неврології. Про деякі периферичні причини запаморочення – їх характеристики й перебіг, а також особливості діагностики та лікування – розповів Михайло Михайлович Орос, д.мед.н., професор, завідувач кафедри неврології, нейрохірургії та психіатрії Ужгородського національного університету.
Характеристики запаморочення
Професор зазначив, що пацієнти часто скаржаться на порушення рівноваги, в більшості випадків маючи на увазі запаморочення. Скарги можна розділити на чотири категорії: справжнє запаморочення (до 50%), пресинкопальний стан (людина відчуває, що зараз втратить свідомість), відчуття «туману» в голові, похитування.
Справжнє запаморочення – відчуття руху свого тіла у просторі або предметів довкола себе, що зазвичай супроводжується порушенням рівноваги. Справжнє запаморочення буває периферичного або центрального генезу. До периферичних уражень належать доброякісне пароксизмальне позиційне запаморочення (близько 35‑45%), хвороба Меньєра (ХМ), вестибулярний нейроніт (ВН), лабіринтит, травма лабіринту, перилімфатична фістула, сифіліс, акустична невринома. Також причиною розвитку такого запаморочення може бути застосування ототоксичних ліків. Центральні ураження включають гостре порушення мозкового кровообігу, хвороби мозочка, синдром задньо-нижньої мозочкової артерії, пухлини мосто-мозочкового кута, епілепсію, цервікальні запаморочення, розсіяний склероз, вестибулярну форму мігрені (Murphy et al., 2022).
Клінічні тестування при запамороченнях
При діагностуванні запаморочення необхідне ретельне обстеження хворих із проведенням різних тестувань та консультацій вузьких фахівців для визначення природи цього стану (Neuhauser, 2016). У пацієнтів із порушенням рівноваги для оцінки спонтанного ністагму використовують окуляри Френзеля (+20D). За допомогою цього оглядового інструменту лікар може точно проаналізувати рухи очей і виявити, чи пошкоджений орган рівноваги.
Фістульну пробу за допомогою пневматичного вушного дзеркала Зігеля (Siegel’s speculum) із застосуванням контрольованого тиску повітря виконують для виявлення пошкоджень периферичної вестибулярної системи (внутрішнього вуха). Калоричний тест зазвичай проводять для діагностування запаморочення центрального генезу шляхом стимуляції зміною температури переважно в латеральному півколовому каналі. Після введення у слуховий канал теплої чи холодної води в нормі виникає ністагм, відсутність якого є ознакою зниження рівня збудливості аналізатора (Whelan, 2023). Ще одним методом дослідження є обертальна проба із використанням крісла Барані (Barany rotation chair test). Цей спеціальний стілець слугує для оцінки функціонального стану вестибулярної системи (Кириченко та співавт., 2021).
Відеоністагмографія – вид обстеження, що базується на реєстрації руху очних яблук та визначає функціональний стан і рівень ураження вестибулярного аналізатора. Особливостями цього методу є фіксація спонтанного та експериментального ністагму й можливість порівняння з обох боків його сили та тривалості (Noreikaite et al., 2024).
Вестибулярний нейроніт
Як зауважив пан Орос, ВН являє собою причину запаморочення периферичного генезу. Це порушення супроводжується ураженням вестибулярного нерва із подальшою появою запаморочення, часто спонтанного. Зазвичай ВН настає раптово й ізольовано, відбувається повне або часткове пригнічення вестибулярної функції одного з лабіринтів. Захворювання рідко супроводжується ураженням слуху. В основі етіології ВН у більшості випадків лежить вірусне ураження вестибулярного нерва, зокрема вірусом простого герпесу типу 1 (який зазвичай перебуває в організмі у латентній формі та активізується при зниженні імунітету) (Furman, Martin, 2008).
Основні клінічні прояви ВН (Smith et al., 2023):
- гостре спонтанне запаморочення;
- нудота, блювання;
- постуральний дисбаланс.
Прояви ВН зазвичай посилюються під час рухів голови і знижуються при її фіксації з закритими очима. Симптоми поступово слабшають протягом наступних днів. У гострій фазі ВН проявляється спонтанним горизонтальним ротаторним ністагмом, спрямованим в один бік. При цьому швидкий компонент ністагму спрямований у протилежний бік. У гострій фазі прояви ВН знижуються за візуальної фіксації. Серед ускладнень даної патології – осцилопсія та постуральний дисбаланс м’язів (Jeong et al., 2013).
Діагностування ВН передбачає оцінку клінічних даних та результатів обстеження. Воно може включати виконання проби Дікса – Холпайка для виключення доброякісного пароксизмального позиційного запаморочення, аналіз ністагму за допомогою електро- й відеоністагмографії, калоричний тест, контрастну магнітно-резонансну томографію (Furman, Martin, 2008; Noreikaite et al., 2024). Окрім того, необхідно провести диференційну діагностику, щоб виключити мозочковий інсульт, інсульт через закупорювання внутрішньої слухової (лабіринтної) артерії, автоімунний лабіринтит, ХМ тощо.
Лікування ВН передбачає застосування кортикостероїдів (метилпреднізолону), противірусних (валацикловіру), антигістамінних засобів, вестибулярну реабілітацію та адекватну ранню мобілізацію пацієнта (Hidayati et al., 2022; Tokle et al., 2020).
Хвороба Меньєра
ХМ є ще однією причиною запаморочення периферичного походження. Але коли саме слід вживати термін «хвороба Меньєра», а коли – «синдром Меньєра»? За словами Михайла Михайловича, діагноз ХМ встановлюють у випадках, коли етіологія недуги неясна. Якщо ж відомо, що такий стан пацієнта є наслідком, наприклад, вертебробазилярної недостатності, йдеться про синдром Меньєра.
До ймовірних причин ХМ належать: алергія, інфекції, імунні (зокрема, автоімунні) впливи, дисбаланс функціонування вегетативної нервової системи, розлади васкуляризації, дегенерація елементів внутрішнього вуха й порушення його гомеостазу внаслідок змін активності клітин (апудоцитів), які продукують біогенні аміни та пептидні гормони (Hauser, 2021). Крім того, ХМ може розвинутися внаслідок травмувань черепа, порушення водно-сольового обміну (наприклад, за тривалого застосування кортикостероїдів), травм під час санаційних операцій і слухополіпшувальних втручань, змін артеріального тиску (частіше гіпотонії), стресів, конфліктних ситуацій тощо.
Класичними ознаками ХМ є періодичні напади вестибулярної декомпенсації, які супроводжуються (Mohseni-Dargah et al., 2023):
- нападоподібним запамороченням із нудотою, блюванням та порушенням рівноваги;
- прогресувальним зниженням слуху (здебільшого однобічним);
- шумом у вухах, що не зникає за перетискання сонної артерії;
- вегетативними розладами.
Напади системного запаморочення тривають від 20 хв до 12 год. Згодом настає період ремісії, що може мати різну тривалість: від декількох днів до року.
Окрім того, ХМ характеризується спонтанним горизонтально-ротаторним ністагмом, падінням у позі Ромберга, що, як і при лабіринтиті, скеровані в бік повільного компоненту ністагму. При поворотах голови у бік ністагму напрямок падіння змінюється.
Діагностика ХМ включає проведення авдіометрії, що допомагає виявити можливі втрати слуху або інші авдіологічні проблеми. Під час дослідження в осіб із ХМ визначається здебільшого горизонтальна, рідше – висхідна або дещо низхідна крива без кістково-повітряного «розриву» (Belinchon et al., 2011). При виконанні калоричного тесту в пацієнтів із ХМ зазвичай констатується гіпорефлексія (Cerchiai et al., 2019).
Лікування ХМ передбачає використання фармакологічних препаратів. Для нівелювання проявів запаморочення при ХМ насамперед призначають антигістамінні засоби. Вестибулярні супресори можуть застосовуватися для усунення гострих нападів. За певними даними, ефективність стероїдів при ХМ становить 60‑80%, діуретиків – 30‑60%, вазоактивних ліків – 30%, аміноглікозидів (інтратимпанальних ін’єкцій) – 70‑90% (Tacikowska et al., 2010). Неабияке значення має дотримання дієти: обмеження вживання рідини, солі, прянощів, а також лікувальна гімнастика. Крім того, при ХМ інколи застосовують терапію позитивним тиском за допомогою пристрою Meniett.
У разі неефективності консервативного лікування вдаються до хірургічних втручань, як-то дренування ендолімфатичного мішка, що застосовується за збереженого слуху з ураженого боку (ефективність – 50‑70%), та селективна невроектомія вестибулярного нерва (ефективність – 80‑90%) (Tacikowska et al., 2010).
Фармакотерапія у пацієнтів із запамороченням
У контексті медикаментозного лікування запаморочення доповідач виділив препарат Арлеверт® (Berlin-Chemie), що містить фіксовану комбінацію дименгідринату (40 мг) та цинаризину (20 мг). Продемонстровано ефективність Арлеверту щодо зменшення проявів запаморочення й усунення вегетативних симптомів за рахунок декількох механізмів дії його компонентів (Swain, 2020).
Дименгідринат – антигістамінний засіб з антихолінергічними властивостями. Це блокатор H1-гістамінових та ацетилхолінових рецепторів, що проникає через гематоенцефалічний бар’єр і впливає на центральні структури стовбура головного мозку, блокуючи холінорецептори та пригнічуючи передачу сигналів у вестибулярних і вегетативних ядрах. Завдяки цим властивостям препарат чинить протиблювотну дію та усуває центральне запаморочення. Своєю чергою цинаризин – селективний антагоніст Н1-рецепторів кальцію та гістаміну, що запобігає гострим нападам периферичного запаморочення або зменшує їх тяжкість, а також нівелює вегетативну симптоматику, як-то шум у вухах, нудота і блювання (Scholtz et al., 2019; Kirtane, 2019).
Ефективність і сприятливу переносимість фіксованої комбінації цинаризину та дименгідринату при лікуванні запаморочення підтверджено даними доказової медицини. Так, задоволеність хворих терапією препаратом Арлеверт® сягала 98%, а рівень побічних явищ при його застосуванні був порівнянним із таким за терапії іншими ліками, зокрема бетагістином, або навіть нижчим (Schremmer et al., 1999). Окрім того, в рандомізованому подвійному сліпому дослідженні з участю пацієнтів з однобічним ВН Арлеверт® достовірно перевершував бетагістин, сприяючи усуненню вегетативних симптомів та зменшенню тяжкості запаморочення на 87% вже на першому тижні; при цьому ефект зберігався на четвертому тижні лікування (рисунок) (Scholtz et al., 2012).
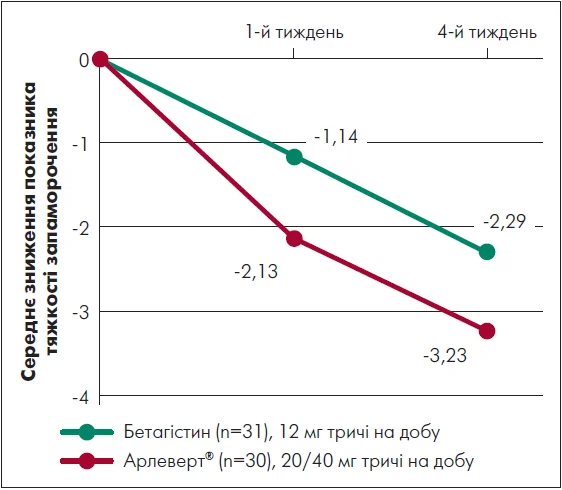 Рисунок. Переваги препарату Арлеверт® порівняно із бетагістином щодо зменшення тяжкості запаморочення в пацієнтів із ВН
Рисунок. Переваги препарату Арлеверт® порівняно із бетагістином щодо зменшення тяжкості запаморочення в пацієнтів із ВН
Адаптовано за A. W. Scholtz et al. (2012)
Спікер підкреслив, що використання Арлеверту допомагає запобігти поширеній на тлі запаморочення інвалідизації пацієнтів, що асоційована із високим ризиком падінь і травмувань. Препарат сприяє зменшенню тяжкості запаморочення, поліпшенню рівноваги й, відповідно, стану хворих, що дозволяє їм залучатися до вестибулярної реабілітації та лікувальної фізкультури, які є важливими заходами для осіб із ХМ.
Таким чином, переваги препарату Арлеверт® полягають у нівелюванні проявів запаморочення і вегетативних симптомів, а також запобіганні виникненню рецидивів та інвалідизації пацієнтів. Це сприяє їх швидкому відновленню та поверненню до нормального життя.
Підготувала Олена Коробка
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 1 (72) 2025 р.




