7 лютого, 2025
Вплив лікування тіоктовою кислотою на нейропатичний біль і біомаркери пошкодження ДНК у пацієнтів із цукровим діабетом
Діабетична полінейропатія (ДПН) є частим мікросудинним ускладненням, яке розвивається в 34% пацієнтів із цукровим діабетом (ЦД) 1 типу та в понад 50% хворих на ЦД 2 типу. На ранніх стадіях діабету ДПН трапляється рідко за ЦД 1 типу, проте її частота може досягати 30% у випадках уперше діагностованого або раннього ЦД 2 типу. Симптоматична ДПН зустрічається в 50% випадків, больова форма становить 30%. Больова ДПН проявляється гіпералгезією, алодинією та болем, що описується як пекучий, колючий, судомний або стріляючий, і зазвичай посилюється вночі. Цей стан суттєво знижує якість життя пацієнтів, спричиняючи порушення сну, обмеження повсякденної активності, збільшення захворюваності та смертності. Класичні знеболювальні засоби за ДПН мають обмежену ефективність і можуть зумовлювати побічні ефекти, тому в клінічній практиці все більше уваги привертає патогенетична терапія.
Одним із патогенетичних напрямів лікування ДПН є боротьба з оксидативним стресом (ОС). Застосування антиоксидантів для впливу на механізми ОС є перспективною стратегією, яка дозволяє зменшити пошкодження нервових клітин і полегшити симптоми нейропатії. З‑поміж антиоксидантів тіоктова (альфа-ліпоєва) кислота є єдиною молекулою, яка демонструє клінічну ефективність і рекомендована для лікування ДПН за ЦД як 1, так і 2 типу.
Тіоктова кислота синтезується в організмі ендогенно, а також надходить із продуктами харчування (червоне м’ясо, буряк, морква, картопля, шпинат, броколі). Вона є кофактором мітохондріальних ферментів, які беруть участь в енергетичному обміні, і захищає клітини від ушкоджувальної дії активних форм кисню (АФК), відновлюючи окиснені форми інших антиоксидантів, зокрема глутатіону. Окрім цього, тіоктова кислота покращує чутливість до інсуліну, знижує ризик мікросудинних ускладнень і сприяє корекції таких супутніх станів, як ожиріння, артеріальна гіпертензія та дисліпідемія.
У дослідженнях in vitro та in vivo також продемонстровано, що тіоктова кислота зменшує кількість ушкоджень ДНК, спричинених генотоксичними агентами.
Останніми десятиліттями в рандомізованих клінічних дослідженнях показано перспективність терапії тіоктовою кислотою в полегшенні нейропатичних симптомів з ефективністю близько 40-60%. Через короткий період напіввиведення тіоктової кислоти в плазмі найефективнішим є внутрішньовенне введення (600 мг/добу), особливо якщо лікування триває від 3 тижнів до 6 місяців. Однак такі схеми терапії можуть бути незручними через необхідність тривалої госпіталізації або щоденних візитів до лікаря. У сучасній клінічній практиці частіше застосовують короткострокові внутрішньовенні курси тривалістю 2-3 тижні з подальшим переходом на тривале пероральне застосування. Проте навіть такі схеми можуть бути складними для багатьох пацієнтів.
Мета цього дослідження – вивчити вплив короткочасного внутрішньовенного лікування тіоктовою кислотою на больову ДПН та маркери пошкодження ДНК у пацієнтів із ЦД.
Матеріали та методи
Дослідження проводили в умовах реальної практики у Вільнюській університетській клініці. Участь взяли 16 пацієнтів із ЦД (1 типу – 6, 2 типу – 10); контрольну групу становили 16 осіб без діабету, яких підбирали за віком і статтю. Середня тривалість діабету дорівнювала 13,7 року для ЦД 1 типу і 15,7 року для ЦД 2 типу. Пацієнти з діабетом отримували внутрішньовенні інфузії тіоктової кислоти в дозі 600 мг/добу протягом 4-9 днів.
Інтенсивність болю вимірювали за допомогою Універсального інструмента оцінки болю (UPAT) до та після лікування. Як маркер пошкодження ДНК визначали концентрацію 8-гідрокси‑2´-дезоксигуанозину (8-OHdG) у плазмі крові. Зразки крові для аналізів брали вранці перед початком лікування та через кілька годин після останньої інфузії. Для статистичного аналізу застосовували парний тест Вілкоксона, результати вважали значущими за р<0,05.
Результати
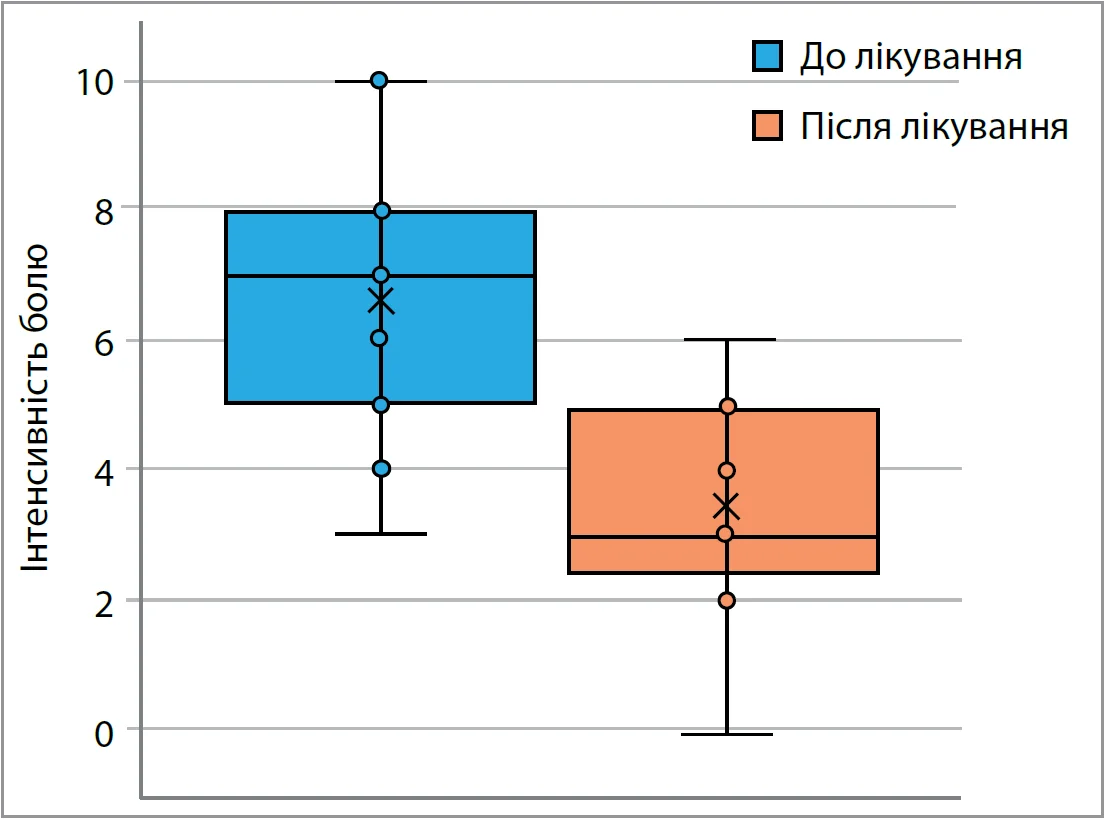
Після курсу лікування тіоктовою кислотою (600 мг/добу протягом 4-9 днів) у пацієнтів із ЦД спостерігали значне зниження інтенсивності болю (рис. 1). У трьох пацієнтів початковий рівень болю становив 0, тому змін після лікування не було зафіксовано. В одного пацієнта початковий рівень болю дорівнював 3 і також залишився без змін. У решти 12 пацієнтів біль зменшився: в деяких випадках – дуже суттєво (приміром, із 10 до 5, з 8 до 2 або з 6 до 0), в інших – помірно (наприклад, із 7 до 6 або з 4 до 2). Загалом інтенсивність болю після лікування була значно нижчою, ніж до початку терапії (p=0,0024).
Початковий рівень болю суттєво не відрізнявся між пацієнтами із ЦД 1 і 2 типу (6,0 проти 7,0 відповідно; p=0,6953), так само як і після лікування (2,5 проти 3,9 відповідно; p=0,0696). Проте зниження болю після лікування було статистично значущим для обох груп: p=0,0265 для пацієнтів із ЦД 1 типу та p=0,0049 для хворих на ЦД 2 типу. Аналіз за статтю також не виявив суттєвих відмінностей: середній рівень болю до лікування в чоловіків становив 6,0, у жінок – 7,1; після лікування – 3,4 та 3,5 відповідно.
Щодо маркера ОС 8-OHdG, то його концентрація в плазмі крові пацієнтів із ЦД була значно нижчою після лікування порівняно з початковими показниками (p=0,0039) (рис. 2).
Рис. 1. Інтенсивність болю в пацієнтів із ЦД до та після лікування тіоктовою кислотою
Рис. 2. Вплив ЦД та лікування тіоктовою кислотою на плазмову концентрацію 8-ОНdG
Обговорення
Лікування тіоктовою кислотою в пацієнтів із ДПН вивчали в багатьох клінічних дослідженнях. Загалом існує консенсус, що тіоктова кислота позитивно впливає на симптоми ДПН та покращує якість життя пацієнтів. Однак ефективність тіоктової кислоти саме в зменшенні нейропатичного болю залишається дискусійною. Деякі метааналізи повідомляють про відсутність ефекту на біль, натомість інші підтверджують, що тіоктова кислота знижує інтенсивність болю. Така розбіжність, імовірно, пов’язана зі способом введення препарату: внутрішньовенні інфузії виявилися значно ефективнішими за пероральний прийом. Біодоступність тіоктової кислоти за перорального прийому становить лише 30%; своєю чергою, внутрішньовенне введення забезпечує вищу пікову концентрацію препарату в плазмі, що, імовірно, є необхідним для відновлення глутатіону в клітинах-мішенях.
Наші результати узгоджуються з дослідженнями, які підтверджують ефективність внутрішньовенного введення тіоктової кислоти в зменшенні нейропатичного болю. Наприклад, у нещодавньому дослідженні після 14-денного курсу лікування біль зменшився на ~3,5 бали. Цікаво, що після перерви в лікуванні біль частково повертався, але знову знижувався після наступного циклу інфузій. Це свідчить про перспективність повторних короткострокових курсів лікування для зменшення симптомів болю. Крім того, попередні дослідження показали, що тривалі курси лікування (6 місяців і довше) не мають суттєвих переваг перед короткостроковими (3-5 тижнів).
Варто зазначити, що тіоктова кислота також демонструє ефективність при інших больових станах, як-от радикулопатія, мігрень, синдром зап’ястного каналу та ідіопатичний біль. Молекулярні механізми дії тіоктової кислоти вивчені доволі добре: вона нейтралізує АФК, відновлює інші антиоксиданти, хелатує метали, пригнічує активацію мікроглії та запобігає пошкодженню мітохондрій.
У нашому дослідженні після лікування тіоктовою кислотою значно знизилася концентрація 8-OHdG – маркера оксидативного ушкодження ДНК. Це свідчить про патогенетичну дію тіоктової кислоти, яка спрямована на зменшення ОС, зокрема на рівні ДНК. Такий ефект підтверджує здатність препарату захищати клітини від дії АФК та сприяти зниженню загального рівня стресу в організмі пацієнтів із ЦД. Зменшення рівня 8-OHdG може також бути індикатором поліпшення метаболічної рівноваги та функції нервових клітин у відповідь на антиоксидантну терапію.
Висновки
Дослідження показало, що в пацієнтів із ЦД 1 та 2 типу з больовою ДПН короткострокове внутрішньовенне лікування тіоктовою кислотою значно зменшує біль і знижує концентрацію маркера ушкодження ДНК. Тіоктова кислота була однаково ефективною в чоловіків і жінок та незалежно від типу діабету.
Список літератури знаходиться в редакції.
Lazutka J. R. et al. Effects of Short-Term Treatment with α-Lipoic Acid on Neuropathic Pain and Biomarkers of DNA Damage in Patients with Diabetes Mellitus. Pharmaceuticals (Basel). 2024 Nov 16; 17 (11): 1538.
Скорочений переклад підготував Олексій Терещенко
Від редакції
На українському фармацевтичному ринку представлений препарат тіоктової кислоти Берлітіон® від німецької компанії «Берлін-Хемі», доступний у двох лікарських формах: Берлітіон® 600 ОД концентрат для приготування розчину для інфузій і Берлітіон® 600 капсули для перорального прийому. Це дозволяє забезпечити комплексний підхід до лікування пацієнтів із ДПН, особливо її больової форми.
Періодичні курси ін’єкційної терапії Берлітіоном є доцільними, коли необхідно досягти максимальної ефективності та швидкого полегшення симптомів. Результати досліджень свідчать, що навіть короткострокове внутрішньовенне введення тіоктової кислоти (600 мг/добу протягом 1-2 тижнів) сприяє суттєвому зменшенню інтенсивності болю, що є одним із ключових викликів для пацієнтів із ДПН.
Після завершення ін’єкційного курсу рекомендований перехід на тривале пероральне застосування препарату, що дозволяє підтримувати ефективність терапії, знижувати рівень ОС і запобігати прогресуванню ДПН. Такий підхід відповідає сучасним стандартам лікування, зосередженим на поєднанні короткотермінових інтенсивних курсів терапії та довготривалої підтримувальній стратегії.
Тіоктова кислота як активний компонент Берлітіону має патогенетичну дію, спрямовану на зменшення ОС, захист клітин від ушкоджень, зокрема на рівні ДНК, і покращення функції нервових волокон. Вона також демонструє позитивний вплив на метаболічний баланс, що включає підвищення чутливості до інсуліну та зниження ризику мікросудинних ускладнень.
Застосування препарату Берлітіон® може сприяти значному покращенню якості життя пацієнтів із больовою ДПН, зменшуючи інтенсивність болю та відновлюючи здатність до повсякденної активності. Це дозволяє не лише полегшити симптоми, а й комплексно впливати на перебіг хвороби.
Берлітіон® від «Берлін-Хемі» – це надійний вибір для пацієнтів із ДПН, що поєднує перевірені ефективність та безпеку, економічну доступність і зручність застосування.
Медична газета «Здоров’я України 21 сторіччя» № 1 (587), 2025 р